
Wetenschap
Trisbuffer als pH door HCL Waarom niet voor natriumacetaat?
1. Tris Buffer en HCl
* tris (tris (hydroxymethyl) aminomethaan) is een zwakke basis met een PKA van 8.1.
* hcl is een sterk zuur.
* hoe het werkt: Wanneer HCl wordt toegevoegd aan Tris, reageert deze met de Tris-basis om het tris-conjugaatzuur (Tris-H+) te vormen. Dit creëert een bufferoplossing met een pH nabij de PKA van Tris (rond 8.1).
2. Natriumacetaatbuffer en HCl
* Natriumacetaat is een zout van een zwak zuur (azijnzuur) en een sterke basis (natriumhydroxide).
* hcl is een sterk zuur.
* Waarom het niet ideaal is: Het toevoegen van HCL aan een natriumacetaatbufferoplossing zou het evenwicht verstoren. De HCL zou reageren met de acetaationen (CH3COO-) om azijnzuur (CH3COOH) te vormen. Dit zou het evenwicht verschuiven naar de zure zijde, wat mogelijk leidt tot een significante daling van de pH en mogelijk de buffercapaciteit van de acetaatbuffer overschrijden.
Belangrijkste verschillen:
* Tris Buffer is ontworpen om te werken met sterke zuren: Door de zwakke basiskarakter kan het protonen (H+) accepteren van sterke zuren zoals HCL, waardoor een buffersysteem ontstaat dat pH -veranderingen verzet.
* Natriumacetaatbuffer is gevoeliger voor sterke zuren: Omdat het een zout van een zwak zuur is, kan het toevoegen van een sterk zuur zoals HCl snel de acetaationen consumeren en het bufferevenwicht verstoren.
Samenvattend:
Hoewel zowel Tris als natriumacetaat nuttig zijn voor het maken van bufferoplossingen, liggen hun sterke punten in verschillende gebieden. TRIS -buffers werken goed met sterke zuren, waardoor ze geschikt zijn voor pH -aanpassingen met behulp van HCL. Natriumacetaatbuffers zijn beter geschikt voor pH -regeling in situaties waarin u veranderingen moet weerstaan vanwege de toevoeging van zwakke zuren of basen.
 Europa plan voor drijvende gasterminals wekt angst voor klimaat
Europa plan voor drijvende gasterminals wekt angst voor klimaat Kustherstel verbeteren door tijdelijk de natuur na te bootsen
Kustherstel verbeteren door tijdelijk de natuur na te bootsen Wat zijn ecosystemen?
Wat zijn ecosystemen?  Welke bijdragen heeft James Harkin geleverd op het gebied van milieuwetenschap?
Welke bijdragen heeft James Harkin geleverd op het gebied van milieuwetenschap?  Onderzoekers ontwikkelen milieuvriendelijke best practices voor het vinden van olie en gas diep onder het aardoppervlak
Onderzoekers ontwikkelen milieuvriendelijke best practices voor het vinden van olie en gas diep onder het aardoppervlak
Hoofdlijnen
- Geklede varkenskarkassen onthullen de geheimen van mummificatie; onderzoek biedt inzichten voor forensische wetenschappers
- Welke eigenschap kan een menselijk nageslacht erven?
- Wat is het geleidende celtype in Phloem?
- Wat is gedrag van dieren gedragsaanpassing?
- Herinneren we ons slechte tijden beter dan goede?
- Welke X- en Y -chromosomen combineren bij het maken?
- Een verklaring van het skeletsysteem
- Onderzoekers analyseren hoe nieuwe anti-MRSA abtibiotica functioneren
- Welke soort heeft de grootste testikels? Groot geheim onthuld door onderzoekers
- Wanneer menselijke expertise het werk van machines verbetert

- Baanbrekende synthesestrategie kan een golf van nieuwe medicinale verbindingen betekenen
- Nieuwe optimalisatiebenadering helpt bij het ontwerpen van lichtere koolstofvezelcomposietmaterialen

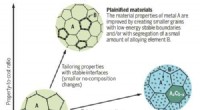
- Verduidelijking belooft veel goeds voor het verbeteren van de duurzaamheid van materialen
- Huidkankermysterie onthuld in yin- en yang-eiwit
 Seven Stages of Early Man
Seven Stages of Early Man  Google koopt Chelsea Market-gebouw in New York voor 2,4 miljard dollar
Google koopt Chelsea Market-gebouw in New York voor 2,4 miljard dollar Onderzoeksintensieve universiteiten in Afrika? Een model om ze te bouwen
Onderzoeksintensieve universiteiten in Afrika? Een model om ze te bouwen Hoe je medewerkers eerlijk beloont en de teamdynamiek verbetert
Hoe je medewerkers eerlijk beloont en de teamdynamiek verbetert  Welke elementen make-up de atmosfeer van de aarde?
Welke elementen make-up de atmosfeer van de aarde?  Vooruitgang in superresolutiemicroscopie
Vooruitgang in superresolutiemicroscopie Welk type binding vindt plaats tussen si en s?
Welk type binding vindt plaats tussen si en s?  Wat gebeurt er in het circuit om hem te laten zien dat de paperclip elektriciteit doorloopt?
Wat gebeurt er in het circuit om hem te laten zien dat de paperclip elektriciteit doorloopt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

