
Wetenschap
Wat is de massa HBR -gas wanneer overtollig H en 1,25 mol BR reageren?
1. Evenwichtige chemische vergelijking:
De evenwichtige chemische vergelijking voor de reactie is:
H₂ (G) + Br₂ (G) → 2HBr (G)
2. Mol -verhouding:
De vergelijking laat zien dat 1 mol Br₂ reageert om 2 mol HBR te produceren.
3. Mol Mol HBR geproduceerd:
Omdat we 1,25 mol BR₂ hebben en de molverhouding 1:2 is, produceren we twee keer zoveel mol HBR:
1,25 mol Br₂ * (2 mol HBr / 1 mol br₂) =2,50 mol HBr
4. Molaire massa van HBR:
De molaire massa van HBR is:
* 1.01 g/mol (h) + 79,90 g/mol (br) =80,91 g/mol
5. Mass van HBR:
Om de massa van HBR te vinden, vermenigvuldigt u de mol HBR door zijn molaire massa:
2.50 mol HBr * 80,91 g/mol = 202,28 g HBR
Daarom is de massa geproduceerde HBR -gas 202,28 gram.
Hoofdlijnen
- Welke macromoleculen vormen vetten oliën en wassen in de biologie?
- Welk ander systeem werkt met het skeletstelsel?
- Hoe gebruiken plantencellen flagella?
- Wat is een voorbeeld van dit algemene type molecuul dat je thuis zou kunnen vinden?
- Wat is RNA -transcriptie en waar vindt het plaats?
- Onderzoekers bestuderen hoe zingende vleermuizen communiceren
- Wat is het verschil tussen hemofilie A en B?
- Morfogenese en de ontwikkeling van levende vormen
- Wat is vergelijkbaar met het weefsel van de planten?
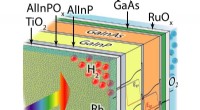
- Nieuw wereldrecord voor directe zonne-watersplitsingsefficiëntie
- Fruitcake-structuur waargenomen in organische polymeren

- 3D-geprint apparaat vindt naald in hooiberg kankercellen door hooi te verwijderen

- Wetenschappers bereiken directe elektrokatalytische reductie van koolstofdioxide, wekt hoop op slimme koolstofafvang

- Digitaliseren en repliceren van de wereld van materialen

 Bioraffinaderijen zullen slechts minimale effecten hebben op de markten voor houtproducten en grondstoffen
Bioraffinaderijen zullen slechts minimale effecten hebben op de markten voor houtproducten en grondstoffen Hoe is een mengsel vastbesloten als heterogeen of homogeen?
Hoe is een mengsel vastbesloten als heterogeen of homogeen?  Beste van vorig jaar:de beste Phys.org-artikelen van 2017
Beste van vorig jaar:de beste Phys.org-artikelen van 2017 3D-geprint apparaat vindt naald in hooiberg kankercellen door hooi te verwijderen
3D-geprint apparaat vindt naald in hooiberg kankercellen door hooi te verwijderen De kern en de mantel van de aarde zijn op een wanordelijke manier gescheiden
De kern en de mantel van de aarde zijn op een wanordelijke manier gescheiden Welke natuurkrachten?
Welke natuurkrachten?  Het EPA-voorstel zou de normen voor roetvervuiling voor het eerst in tien jaar veranderen:wat we weten
Het EPA-voorstel zou de normen voor roetvervuiling voor het eerst in tien jaar veranderen:wat we weten  Algoritme kan helpen de populariteit van posts op sociale media te vergroten
Algoritme kan helpen de populariteit van posts op sociale media te vergroten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


