
Wetenschap
Wat maakt de stroom van ionen in een elektrochemische cel mogelijk?
Hier is hoe het werkt:
* elektrochemische cellen bestaan uit twee halve cellen, die elk een elektrode bevatten ondergedompeld in een elektrolytoplossing.
* elektrolyten zijn oplossingen die ionen bevatten die een elektrische stroom kunnen vervoeren.
* Redox -reacties komen op bij de elektroden, wat resulteert in de overdracht van elektronen.
* Om elektrische neutraliteit te behouden en de stroomstroom toe te staan, moeten ionen tussen de halve cellen bewegen.
De zoutbrug of poreus membraan dient deze cruciale rol door:
* een pad voor ionmigratie bieden tussen de twee halve cellen.
* Het handhaven van elektrische neutraliteit in de cel door ionen uit de halve cel te laten stromen met een overmaat positieve lading naar de halve cel met een overmaat negatieve lading.
* Het voorkomen van directe mengen van de elektrolytoplossingen In de twee halve cellen, die kunnen leiden tot ongewenste reacties.
Soorten ionenstroom:
* anionen (negatief geladen ionen) beweeg naar de anode (positieve elektrode).
* kationen (Positief geladen ionen) beweeg naar de kathode (negatieve elektrode).
Samenvattend is de zoutbrug of poreus membraan essentieel voor de stroom van ionen in een elektrochemische cel, waardoor de overdracht van lading en de voortzetting van de redoxreacties mogelijk is.
 Onderzoekers ontwikkelen molecuul dat kan leiden tot eerste synthetische antimalariamiddel in één dosis
Onderzoekers ontwikkelen molecuul dat kan leiden tot eerste synthetische antimalariamiddel in één dosis Maken ijzer en chloor ionische verbindingen?
Maken ijzer en chloor ionische verbindingen?  De lijnen in het heldere lijnspectrum van een atoom zijn te wijten aan wat?
De lijnen in het heldere lijnspectrum van een atoom zijn te wijten aan wat?  Zijn lood en pyriet vergelijkbaar wat betreft elektrische geleidbaarheid?
Zijn lood en pyriet vergelijkbaar wat betreft elektrische geleidbaarheid?  Licht werpen op hoe stedelijk vuil de chemische reacties in steden beïnvloedt
Licht werpen op hoe stedelijk vuil de chemische reacties in steden beïnvloedt
 Onderzoekers kwantificeren koolstofveranderingen in weidegronden in Sierra Nevada
Onderzoekers kwantificeren koolstofveranderingen in weidegronden in Sierra Nevada NASA ziet krachtige tropische cycloon Gita in de Stille Zuidzee
NASA ziet krachtige tropische cycloon Gita in de Stille Zuidzee Alledaagse toepassingen van biologie
Alledaagse toepassingen van biologie Nieuwe steden kunnen miljoenen kwetsbaarder maken voor klimaatverandering
Nieuwe steden kunnen miljoenen kwetsbaarder maken voor klimaatverandering Wetenschappers vinden stabiele zeespiegel tijdens laatste interglaciaal
Wetenschappers vinden stabiele zeespiegel tijdens laatste interglaciaal
Hoofdlijnen
- Is Yellow Fever -virus DNA of RNA?
- Cowpea beschermd tegen een verwoestende plaag, gratis voor kleine Afrikaanse boeren
- Tand snel, tand nieuwsgierig? Nieuwe studie onthult een nieuwe benadering van plantaardig dieet en unieke dinosaurussen met lange nek
- Wat is de functie van de pellet?
- Wat wegen en hersenen weegt?
- Wat houdt ons tegen om algen en anaërobe bacteriën naar Mars te lanceren om te beginnen met terravorming voor mogelijke toekomstige bewoning?
- Waar begint de assemblage van ribosomen?
- Hoe zou u de biologie definiëren en relateren aan de belangrijkste divisies?
- Waarom is belangrijk voor het wortel- en schietsysteem van planten om samen te werken?
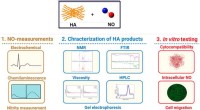
- Onderzoekers gebruiken stikstofmonoxidevangers om triple-negatieve borstkanker aan te pakken
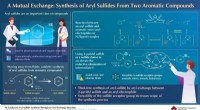
- Het synthetiseren van arylsulfiden uit niet-ruikende, niet-toxische verbindingen
- Een sleutel tot calciumsignalering:structuur van de menselijke IP3R type 3 in zijn ligandvrije toestand

- Video:Wat zijn forever chemicaliën, en gaan ze voor altijd mee?

- Spannende nieuwe ontwikkelingen voor polymeren gemaakt van afvalzwavel

 Planten die giftig zijn voor doosschildpadden
Planten die giftig zijn voor doosschildpadden  Nieuwe twijfels over de Neanderthaler herkomst van Nerja grotkunst
Nieuwe twijfels over de Neanderthaler herkomst van Nerja grotkunst Wat zijn de cellen opgeslagen in eierstokken?
Wat zijn de cellen opgeslagen in eierstokken?  Is het oké om AI te gebruiken om de stem van uw kind te klonen en een politieke boodschap over te brengen?
Is het oké om AI te gebruiken om de stem van uw kind te klonen en een politieke boodschap over te brengen?  Zo ziet het eruit als een zwart gat een ster eet
Zo ziet het eruit als een zwart gat een ster eet  Mangrovebossen vangen drijvend afval op
Mangrovebossen vangen drijvend afval op Indiase wetenschappers maken diepste radiobeelden van de zon
Indiase wetenschappers maken diepste radiobeelden van de zon Wetenschappers maken biologisch afbreekbare microbeads van cellulose
Wetenschappers maken biologisch afbreekbare microbeads van cellulose
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

