
Wetenschap
Waarom heeft fluor een kleinere atoomradius dan zuurstof en chloor?
Dit is waarom:
* atomaire straal verwijst naar de grootte van een neutraal atoom. In dit geval heeft fluor (F) een kleinere atoomradius dan zuurstof (O) en chloor (CL).
* ionische straal verwijst naar de grootte van een ion (een atoom dat elektronen heeft gewonnen of verloren). Fluor, zuurstof en chloor vormen allemaal negatieve ionen (anionen).
Waarom is de atoomradius van fluor kleiner?
* Effectieve nucleaire lading: Fluor heeft een kleinere atoomradius omdat het een hogere effectieve nucleaire lading heeft. Dit betekent dat de kern van het fluoratoom sterker aan de elektronen trekt, ze dichter bij de kern trekt en het atoom kleiner maakt.
* Aantal elektronenschalen: Alle drie de elementen bevinden zich in dezelfde periode (rij) van de periodieke tabel, wat betekent dat ze hetzelfde aantal elektronenschalen hebben. Fluor heeft echter de meeste protonen in zijn kern, wat leidt tot een sterkere aantrekkingskracht voor de elektronen.
Waarom is de ionische straal van fluor kleiner dan zuurstof en chloor?
* Elektronenconfiguratie: Fluor, zuurstof en chloor krijgen allemaal elektronen om hun anionen te vormen. Fluor krijgt echter slechts één elektron, terwijl zuurstof twee wint en chloor drie wint.
* elektronenafstoting: Met meer elektronen is de afstoting tussen hen groter in zuurstof- en chloor -anionen, waardoor hun ionische stralen groter worden.
Samenvattend:
* Fluor heeft een kleinere atoomradius dan zuurstof en chloor omdat het een sterkere effectieve nucleaire lading heeft.
* Fluor's ionische straal is kleiner dan die van zuurstof en chloor omdat het minder elektronen in zijn anion heeft.
 Inktvishuid inspireert tot het maken van een ruimtedeken van de volgende generatie
Inktvishuid inspireert tot het maken van een ruimtedeken van de volgende generatie Pijnloze huidpleister verzamelt vloeistof voor diagnostische tests
Pijnloze huidpleister verzamelt vloeistof voor diagnostische tests Bier brouwen dat langer vers smaakt
Bier brouwen dat langer vers smaakt Hoe ki geformuleerd voor jodium ontbinding?
Hoe ki geformuleerd voor jodium ontbinding?  Welke kernreactie combineert gas om helium te vormen en produceert het grootste deel van de energie van de zon?
Welke kernreactie combineert gas om helium te vormen en produceert het grootste deel van de energie van de zon?
 San Francisco verslikt zich in giftige lucht terwijl bosbranden woeden
San Francisco verslikt zich in giftige lucht terwijl bosbranden woeden Hoe wordt sneeuwval gemeten? Een meteoroloog legt uit hoe vrijwilligers winterstormen tellen
Hoe wordt sneeuwval gemeten? Een meteoroloog legt uit hoe vrijwilligers winterstormen tellen Gletsjers krimpen en verdwijnen snel:50 jaar gletsjerverandering in Montana
Gletsjers krimpen en verdwijnen snel:50 jaar gletsjerverandering in Montana Wintertarwe haalbaar dekgewas voor Rolling Plains-katoen
Wintertarwe haalbaar dekgewas voor Rolling Plains-katoen Betekenis van Pacific Northwest Native American Orca Design
Betekenis van Pacific Northwest Native American Orca Design
Hoofdlijnen
- Het verschil tussen glycolyse en gluconeogenese
- Wat is het verschil tussen een dominante eigenschap en recessieve eigenschap?
- Hoe zou een dieren zijn extra opgeslagen suiker vrijgeven?
- Wie zijn wetenschappers die vaccins ontwikkelen?
- Hoe je hersenen werken
- Verschillen tussen Protozoa en Protisten
- Een evolutiepatroon waarin iets verschillende soorten evolueren van één gemeenschappelijke voorouder?
- Een vaccin voor eetbare planten? nieuwe gewasbeschermingsmethode in zicht
- Maaien of niet maaien:Overlastgroei van waterplanten bij de wortel aanpakken
- Ontwerpen van selectieve reacties om biologische processen te moduleren

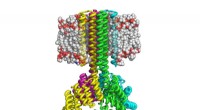
- Wetenschappers creëren vanuit het niets complexe transmembraaneiwitten
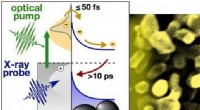
- Wetenschappers maken spontane snapshots van elektronen die licht oogsten op atomaire schaal
- Hittegeharde magnesiumlegering een sterke keuze voor implantaten
- Machine learning maakt een optimaal ontwerp van anti-biofouling polymere borstelfilms mogelijk

 Hoe werkt een ecosysteem?
Hoe werkt een ecosysteem?
Planten of planten zijn de belangrijkste producenten van een ecosysteem. Ze absorberen zonlicht en koolstofdioxide (CO2) uit de atmosfeer en gebruiken water en mineralen uit de grond om hun eigen voedsel te maken. Ze schei
 Wil je de klimaatverandering aanpakken? Pak eerst je voedselverspilling aan
Wil je de klimaatverandering aanpakken? Pak eerst je voedselverspilling aan Aardbevingen aan de oostkust komen niet vaak voor, maar worden door miljoenen mensen gevoeld. Dit is wat u moet weten
Aardbevingen aan de oostkust komen niet vaak voor, maar worden door miljoenen mensen gevoeld. Dit is wat u moet weten  Wanneer een monster van 20,0 g CoCl2 - 6H2O in een oven wordt gedroogd totdat het droog is, wordt de massa kobaltchloride verkregen?
Wanneer een monster van 20,0 g CoCl2 - 6H2O in een oven wordt gedroogd totdat het droog is, wordt de massa kobaltchloride verkregen?  De 210 miljoen jaar oude Smok verpletterde botten als een hyena
De 210 miljoen jaar oude Smok verpletterde botten als een hyena Wat wil de kern van één atoom elektronen in de buurt van atoom doen?
Wat wil de kern van één atoom elektronen in de buurt van atoom doen?  In ruimtecapsules, kleine ruimte maar grote verbetering
In ruimtecapsules, kleine ruimte maar grote verbetering Macho-make-up:nieuw onderzoek naar hoe cosmetica de aantrekkelijkheid bij mannen vergroot
Macho-make-up:nieuw onderzoek naar hoe cosmetica de aantrekkelijkheid bij mannen vergroot
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

