
Wetenschap
Welke is groter in grootte aluminium atoom of chlooratoom?
Dit is waarom:
* Atomische straal: Atomische straal verwijst naar de grootte van een atoom. Aluminium heeft een grotere atoomradius dan chloor.
* Elektronenconfiguratie: Aluminium heeft drie elektronen in de buitenste schaal, terwijl chloor er zeven heeft. Dit betekent dat de buitenste elektronen van aluminium verder van de kern zijn, waardoor het atoom groter wordt.
* Afschermingseffect: De binnenste elektronen in aluminium beschermen de buitenste elektronen van de trek van de kern, die de atoomradius verder verhoogt.
Samenvattend: Aluminium heeft een grotere atoomradius omdat het minder elektronen heeft in zijn buitenste schaal en een groter afschermingseffect.
 Slim materiaal maakt nieuwe toepassingen mogelijk in autonoom rijden en robotica
Slim materiaal maakt nieuwe toepassingen mogelijk in autonoom rijden en robotica Wat is de pH van een stof met een pOH van 4,8?
Wat is de pH van een stof met een pOH van 4,8?  Studie verandert lang gekoesterde concepten van celdecodering
Studie verandert lang gekoesterde concepten van celdecodering Onthulling van een nieuwe AAK1-remmer:hoe chemische proteomics therapeutisch potentieel ontsluiten
Onthulling van een nieuwe AAK1-remmer:hoe chemische proteomics therapeutisch potentieel ontsluiten  Hoe te bepalen of iets is verminderd of geoxideerd
Hoe te bepalen of iets is verminderd of geoxideerd
 Nieuwe studie toont voordelen van ondergewaardeerde kwelder aan
Nieuwe studie toont voordelen van ondergewaardeerde kwelder aan Index onthult integriteitsproblemen voor veel van 's werelds bossen
Index onthult integriteitsproblemen voor veel van 's werelds bossen Het voorspellen van de variabele opname van koolstofdioxide door de oceaan
Het voorspellen van de variabele opname van koolstofdioxide door de oceaan Elektronische luchtreinigingstechnologie kan onbedoelde verontreinigende stoffen genereren
Elektronische luchtreinigingstechnologie kan onbedoelde verontreinigende stoffen genereren Duitsland bereikt klimaatdoel dankzij pandemie
Duitsland bereikt klimaatdoel dankzij pandemie
Hoofdlijnen
- Is er een aanpassing voor de spijsvertering?
- De functies van de linker temporale kwab
- Is een Dall Sheep Herbivore Carnivore of Omnivore waarom?
- Waarom Afrikaanse wetenschappers de genen van Afrikaanse soorten bestuderen en hoe ze dat doen
- Vogelgriep:hoe het zich verspreidt en wat u moet weten over deze uitbraak
- Wat is extraverte eigenschap?
- Biologische leeftijd verklaart variatie in reacties op stress
- Welke plantenaanpassing is slijmerig sappige weefselwinkels water in het droge seizoen?
- Hoe push-pull begeleidende gewassen helpen bij het beheersen van de verwoestende herfstplaag van legerwormen
- Team ontwikkelt nieuwe methode om hernieuwbaar acrylonitril te produceren

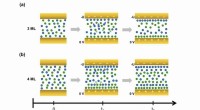
- Wetenschappers ontwikkelen real-time techniek voor het bestuderen van ionische vloeistoffen op elektrode-interfaces
- Het geheim van de Stradivari-viool bevestigd

- Cementloze vliegasbinder maakt beton groen

- Een stap in de richting van metaal-organische raamwerksynthese
 Hoe zal de snelheid van de geluidsgolf veranderen als het temperatuurmedium stijgt?
Hoe zal de snelheid van de geluidsgolf veranderen als het temperatuurmedium stijgt?  Nanodeeltjes die zowel MRI als fluorescerende beeldvorming mogelijk maken, kunnen kanker volgen, andere ziekten
Nanodeeltjes die zowel MRI als fluorescerende beeldvorming mogelijk maken, kunnen kanker volgen, andere ziekten 15 graden South 150 Oostzee?
15 graden South 150 Oostzee?  Wie heeft videogames uitgevonden?
Wie heeft videogames uitgevonden?  Welk kenmerk van grote biologische moleculen verklaart hun grote diversiteit?
Welk kenmerk van grote biologische moleculen verklaart hun grote diversiteit?  De toekomst van innovatie in consumententechnologie
De toekomst van innovatie in consumententechnologie Onderzoekers verplaatsen grafeenelektronica naar 3D
Onderzoekers verplaatsen grafeenelektronica naar 3D Onderzoekers ontwikkelen lijm op waterbasis die kan worden gerecycled door de pH te veranderen
Onderzoekers ontwikkelen lijm op waterbasis die kan worden gerecycled door de pH te veranderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

