
Wetenschap
Welke elementen combineren om een covalente verbinding te vormen?
* niet -metalen: Dit zijn elementen aan de rechterkant van de periodiek systeem (exclusief waterstof). Ze hebben de neiging om een hoge elektronegativiteit te hebben, wat betekent dat ze elektronen sterk aantrekken.
* Elektronen delen: In plaats van elektronen over te dragen zoals in ionische verbindingen, delen niet -metalen hun valentie -elektronen om een stabiele elektronenconfiguratie te bereiken, die lijkt op een edelgas.
Voorbeelden van covalente verbindingen:
* water (h₂o): Waterstof en zuurstof delen elektronen om stabiele bindingen te vormen.
* koolstofdioxide (co₂): Koolstof deelt elektronen met twee zuurstofatomen.
* methaan (ch₄): Koolstof deelt elektronen met vier waterstofatomen.
Sleutelpunten:
* Covalente bindingen worden meestal gevormd tussen twee niet -metalen.
* De gedeelde elektronen worden aangetrokken door beide kernen, waardoor een sterke binding ontstaat.
* Covalente verbindingen bestaan vaak als moleculen, die groepen atomen zijn die bij elkaar worden gehouden door covalente bindingen.
 Wat gebeurt er als zilvernitraat aan bariumchloride wordt toegevoegd?
Wat gebeurt er als zilvernitraat aan bariumchloride wordt toegevoegd?  Uranium ter vervanging van plastic? Een doorbraak in de chemie kan de weg vrijmaken voor nieuwe materialen
Uranium ter vervanging van plastic? Een doorbraak in de chemie kan de weg vrijmaken voor nieuwe materialen  Hoe zou men 2 m oplossing van een verbinding maken?
Hoe zou men 2 m oplossing van een verbinding maken?  Wat betekent nona in de chemie?
Wat betekent nona in de chemie?  Chemici ontwikkelen hydrogelsnaren met behulp van verbindingen die in zeedieren worden gevonden
Chemici ontwikkelen hydrogelsnaren met behulp van verbindingen die in zeedieren worden gevonden
 Horizontale winden worden belangrijke verhuizers van koolstofdioxide tijdens koude fronten
Horizontale winden worden belangrijke verhuizers van koolstofdioxide tijdens koude fronten Hoe communiceren apen?
Hoe communiceren apen?  Het aantal dat klimaatactie in overdrive zou kunnen brengen
Het aantal dat klimaatactie in overdrive zou kunnen brengen Het Duitse kabinet tekent plannen af om CO2-afvang mogelijk te maken
Het Duitse kabinet tekent plannen af om CO2-afvang mogelijk te maken  Chinese honger naar het meest stinkende fruit bedreigt Maleisische bossen
Chinese honger naar het meest stinkende fruit bedreigt Maleisische bossen
Hoofdlijnen
- Afrikaanse boeren kijken naar het verleden en de toekomst om de klimaatverandering aan te pakken
- Wanneer vormden bacteriën?
- Waar is een cellulosespons van gemaakt?
- Stadia van een typische celcyclus
- Wat observeren wetenschapper het meest?
- Delen van een dierencel voor kinderen
- Leg uit hoe wordt het dubbele helixmodel van DNA gebouwd op onderzoek Rosalind Franklin?
- Welk type reproductie waarvoor slechts één ouder nodig is?
- Waarom dat lange gezicht? Paarden en mensen delen gezichtsuitdrukkingen
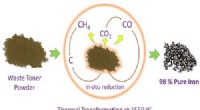
- Strijkijzer uit printerafvaltoner trekken
- Een nieuwe miniatuuroplossing voor het opslaan van duurzame energie
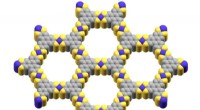
- Kristaloorlogen:onderzoek kan leiden tot efficiëntere methoden voor kristaltechnologie

- Nieuw maskermateriaal kan nanodeeltjes van virusgrootte verwijderen

- Fosfor:350 jaar na zijn ontdekking, dit vitale element raakt op

 TV-industrieshow begroet smartphone-, Facebook-tijdperk
TV-industrieshow begroet smartphone-, Facebook-tijdperk  Groot oppervlak geeft superkrachten aan ultraporeuze materialen
Groot oppervlak geeft superkrachten aan ultraporeuze materialen Wat zijn de drie soorten lipiden die in voedingsmiddelen worden gevonden?
Wat zijn de drie soorten lipiden die in voedingsmiddelen worden gevonden?  Mitsubishi Motors:Schandaal getroffen derde wiel in Ghosns alliantie
Mitsubishi Motors:Schandaal getroffen derde wiel in Ghosns alliantie Zelfs in de best-case emissiescenario's, zeespiegel kan nog stijgen tot 2300
Zelfs in de best-case emissiescenario's, zeespiegel kan nog stijgen tot 2300 Oude kwikvervuiling nog steeds een probleem in de wateren van de weiden van New Jersey
Oude kwikvervuiling nog steeds een probleem in de wateren van de weiden van New Jersey Wetenschappers werpen licht op het conserveringsmysterie van wapens van het terracotta leger
Wetenschappers werpen licht op het conserveringsmysterie van wapens van het terracotta leger Met nanokristallen gecoate vezels kunnen verspilde energie verminderen
Met nanokristallen gecoate vezels kunnen verspilde energie verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

