
Wetenschap
Natrium en chloor bevinden zich in dezelfde periode op periodieke tabel Verklaar het verschil in hun afmetingen?
* Atomische structuur: Terwijl je een periode van links naar rechts beweegt, neemt het aantal protonen in de kern toe. Deze verhoogde positieve lading trekt de negatief geladen elektronen sterker aan en trekt de elektronenwolk dichter bij de kern.
* natrium versus chloor:
* natrium (NA): Heeft 11 protonen en 11 elektronen. Het buitenste elektron bevindt zich in de 3s orbital.
* chloor (CL): Heeft 17 protonen en 17 elektronen. De buitenste elektronen bevinden zich in de 3S- en 3P -orbitalen.
* Effect op maat: Omdat chloor een grotere nucleaire lading (meer protonen) heeft, worden de elektronen nauwer getrokken. Dit maakt chloor kleiner dan natrium, hoewel beide elementen hun buitenste elektronen in hetzelfde energieniveau hebben (3e energieniveau).
Samenvattend:
* natrium (NA): Grotere atoomgrootte als gevolg van een zwakkere aantrekkingskracht tussen zijn kern en buitenste elektron.
* chloor (CL): Kleinere atoomgrootte als gevolg van een sterkere aantrekkingskracht tussen zijn kern en buitenste elektronen.
Laat het me weten als je nog andere vragen hebt!
 Hoeveel moleculen koolstofdioxide worden er gebruikt om 1 molecuul te maken?
Hoeveel moleculen koolstofdioxide worden er gebruikt om 1 molecuul te maken?  Welke vloeistoffen kunnen mengen met water?
Welke vloeistoffen kunnen mengen met water?  Een bijgewerkt begrip van het synthetiseren van chemicaliën met toegevoegde waarde
Een bijgewerkt begrip van het synthetiseren van chemicaliën met toegevoegde waarde Met welk type elektronen hebben ionische bindingen te maken?
Met welk type elektronen hebben ionische bindingen te maken?  Wat zullen de waarnemingen zijn als de zinknitraatoplossing aan de loodoplossing wordt toegevoegd?
Wat zullen de waarnemingen zijn als de zinknitraatoplossing aan de loodoplossing wordt toegevoegd?
 De vorming van mest uit bladeren is een fysieke verandering?
De vorming van mest uit bladeren is een fysieke verandering?  De luchtvervuiling in de West Midlands veroorzaakt jaarlijks tot 2.300 vroegtijdige sterfgevallen, blijkt uit onderzoek
De luchtvervuiling in de West Midlands veroorzaakt jaarlijks tot 2.300 vroegtijdige sterfgevallen, blijkt uit onderzoek  Hoe burgerwetenschap passieve leerlingen transformeert in betrokken wetenschappers
Hoe burgerwetenschap passieve leerlingen transformeert in betrokken wetenschappers  Hoe insecten geuren opsporen door op microschaal winden te navigeren
Hoe insecten geuren opsporen door op microschaal winden te navigeren  Welk woord verwijst naar de oppervlakte -kenmerken?
Welk woord verwijst naar de oppervlakte -kenmerken?
Hoofdlijnen
- Naar welk type cel behoort een ribosoom?
- Termieten houden van het broeikaseffect, het tempo van hun houtkauwen wordt aanzienlijk sneller bij warmer weer
- Chili vecht om een favoriete mossel te redden
- De meest directe vorm van DNA -analyse is?
- Is de wetenschap slaap aan het uitfaseren?
- Verklaarde dat de overerving van verworven eigenschappen in de loop van de tijd verandering bij een soort veroorzaakte?
- Studie onderstreept nieuwe strategieën om resistente bacteriën te bestrijden
- Hoe vrouwelijke valse weduwenspinnen hun 'spidey-zintuigen' gebruiken om partners aan te trekken - onderzoek dit
- Kunnen darmbacteriën de volgende sportdrank worden?
- Video:Er zit goud in zeewater! Kunnen we het extraheren?

- Hydrogel kan diabetische zweren helpen genezen
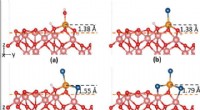
- Supercomputermodellen beschrijven de rol van chloriden bij corrosie
- Nieuw begrip van de synthese van antibiotica
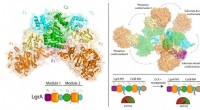
- Nieuwe watersplitsingskatalysator kan het gemakkelijker maken om zonnebrandstof te genereren

 Is het beter om te straffen of te belonen om een coöperatieve samenleving op te bouwen?
Is het beter om te straffen of te belonen om een coöperatieve samenleving op te bouwen?  Gebruik maken van een openbaar toilet? Masker op!
Gebruik maken van een openbaar toilet? Masker op!  Gebrek aan subsidies van financieringsinstanties grootste belemmering voor publicatie van OA in natuurwetenschappen, studievondsten
Gebrek aan subsidies van financieringsinstanties grootste belemmering voor publicatie van OA in natuurwetenschappen, studievondsten Wat is het verschil tussen een aminozuur en nucleïnezuur?
Wat is het verschil tussen een aminozuur en nucleïnezuur?  Kunnen steden slimmer omgaan met extreem weer?
Kunnen steden slimmer omgaan met extreem weer? Koe maskers? Landbouwbedrijf probeert methaanabsorberend draagbaar apparaat
Koe maskers? Landbouwbedrijf probeert methaanabsorberend draagbaar apparaat  Hoe satelliethalsbanden de weg vrijmaken voor slimmere bescherming van saiga-antilopen
Hoe satelliethalsbanden de weg vrijmaken voor slimmere bescherming van saiga-antilopen  Facebook laat gebruikers, net als MySpace, de volledige naam weergeven
Facebook laat gebruikers, net als MySpace, de volledige naam weergeven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

