
Wetenschap
Wat is de empirische formule van een verbinding die 53,73 procent Fe en 46,27 s bevat?
1. Ga uit van een 100 g monster
Hierdoor worden de percentages direct vertaald naar grams:
* 53.73 G FE
* 46.27 G S
2. Converteer grams naar mollen
Verdeel de massa van elk element door zijn molaire massa:
* Fe:53.73 g / 55.845 g / mol =0,962 mol Fe
* S:46.27 g / 32.065 g / mol =1.443 mol s
3. Vind de molverhouding
Verdeel elke molwaarde door de kleinste molwaarde:
* Fe:0,962 mol / 0,962 mol =1
* S:1.443 mol / 0,962 mol =1,5
Omdat we hele getallen nodig hebben voor de empirische formule, vermenigvuldig je beide met 2:
* Fe:1 * 2 =2
* S:1.5 * 2 =3
4. Schrijf de empirische formule
De empirische formule is fe₂s₃ .
 Wat vertegenwoordigt een enkele rechte lijn (-CH3) die zich uitstrekt van een atoomsymbool?
Wat vertegenwoordigt een enkele rechte lijn (-CH3) die zich uitstrekt van een atoomsymbool?  Nieuwe geleidende, op katoen gebaseerde vezel ontwikkeld voor slim textiel
Nieuwe geleidende, op katoen gebaseerde vezel ontwikkeld voor slim textiel  Lijst met geleiders
Lijst met geleiders  Hoeveel protonen zitten er in azijn?
Hoeveel protonen zitten er in azijn?  Welk niveau van eiwitstructuur kan worden gestabiliseerd door covalente bindingen?
Welk niveau van eiwitstructuur kan worden gestabiliseerd door covalente bindingen?
 Oplossingen voor bodemverontreiniging
Oplossingen voor bodemverontreiniging Studie onderzoekt de impact van zwarte mangroven op het voedselweb van kwelder
Studie onderzoekt de impact van zwarte mangroven op het voedselweb van kwelder Ondanks de voordelen van de stadsboom, Californische stedelijke luifeldekking per hoofd van de bevolking het laagst in de VS
Ondanks de voordelen van de stadsboom, Californische stedelijke luifeldekking per hoofd van de bevolking het laagst in de VS Tyfoon Shanshan klemt Japanse kust vast, Tokio sparen
Tyfoon Shanshan klemt Japanse kust vast, Tokio sparen NASA vindt kortstondige Fausto snel vervaagd
NASA vindt kortstondige Fausto snel vervaagd
Hoofdlijnen
- Nieuw onderzoek laat zien hoe genen aan en uit gaan
- Welk domein multicellulaire fotosynthetische organismen?
- Hoe kunnen slechts 4 basen in rna instructies bevatten voor 20 aminozuren?
- Welke organismen die organische bronnen van koolstof en energie vereisen?
- Onderzoek onthult hoe cellen zich herbouwen na mitose
- Waarom is stikstof belangrijk voor de mens?
- Zenuwen controleren de bacteriële gemeenschap van het lichaam
- Hoeveel kost het GC -gehalte van het menselijk genoom?
- Onderzoekers gebruiken genoomanalyse om te begrijpen hoe koningspinguïns op de Crozet-eilanden kwamen broeden
- Bladaderstructuur kan de sleutel zijn tot het verlengen van de levensduur van de batterij

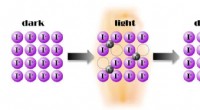
- Lichtgestuurd stroomtransport door geladen atomen voor het eerst gedemonstreerd
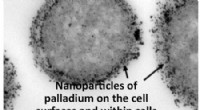
- Onderzoekers identificeren goedkopere, groenere katalysator voor de verwerking van biobrandstoffen
- Kunstmatige cyanobacteriële biofilm kan de productie van groene ethyleen meer dan een maand ondersteunen

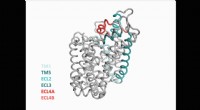
- Neurowetenschappers ontdekken nieuwe structuur van belangrijk eiwit in de hersenen
 Wat gebeurt er als een gletsjer smelt?
Wat gebeurt er als een gletsjer smelt?
Naarmate de gemiddelde wereldtemperatuur stijgt, smelten gletsjers en trekken ze de valleien terug die ze naar beneden zijn gegaan. Wanneer gletsjers verdwijnen, wordt het landschap niet meer aangetast door to
 Braziliaanse onderzoekers ontdekken zes nieuwe soorten zijdemiereneter
Braziliaanse onderzoekers ontdekken zes nieuwe soorten zijdemiereneter Hoe groene daken steden kunnen helpen overtollig regenwater weg te sponzen
Hoe groene daken steden kunnen helpen overtollig regenwater weg te sponzen Bescherming van het recht om vergeten te worden in het tijdperk van blockchain
Bescherming van het recht om vergeten te worden in het tijdperk van blockchain Is hcl een verbinding of element?
Is hcl een verbinding of element?  Diversiteit bij non-profitorganisaties voor podiumkunsten koppelen aan marketing, financiering, locatie
Diversiteit bij non-profitorganisaties voor podiumkunsten koppelen aan marketing, financiering, locatie Plotselinge overstromingen die enorme hoeveelheden microplastics van rivieren naar zee sturen
Plotselinge overstromingen die enorme hoeveelheden microplastics van rivieren naar zee sturen Chemische reacties gefilmd op het niveau van één molecuul
Chemische reacties gefilmd op het niveau van één molecuul
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

