
Wetenschap
Wanneer dampdruk gelijk is aan atomosferisch, wat is de vloeistof?
Dit is waarom:
* dampdruk: Dit is de druk die wordt uitgeoefend door de damp van een vloeistof wanneer deze in evenwicht is met zijn vloeibare fase. In wezen is het de druk van de gasmoleculen die uit het oppervlak van de vloeistof ontsnappen.
* Atmosferische druk: Dit is de druk die wordt uitgeoefend door het gewicht van de lucht boven ons.
kookpunt: Het kookpunt van een vloeistof is de temperatuur waarbij de dampdruk gelijk is aan de omliggende atmosferische druk. Op dit punt hebben de moleculen van de vloeistof voldoende energie om de aantrekkelijke krachten te overwinnen die ze bij elkaar houden en overgaan in de gasfase. Bubbels vormen zich in de vloeistof, stijgen naar het oppervlak en ontsnappen.
Kortom: Wanneer dampdruk en atmosferische druk gelijk zijn, bevindt de vloeistof zich op het kookpunt en verandert actief in een gas.
 Video:Geologen verkennen de geschiedenis van grotijs
Video:Geologen verkennen de geschiedenis van grotijs 'Peking Man' ouder dan gedacht; op de een of andere manier aangepast aan de kou
'Peking Man' ouder dan gedacht; op de een of andere manier aangepast aan de kou  Hoe zich te ontdoen van zeewier
Hoe zich te ontdoen van zeewier  NASA vindt Kiko verzwakking in de oostelijke Stille Oceaan
NASA vindt Kiko verzwakking in de oostelijke Stille Oceaan Realistisch nieuw model wijst de weg naar efficiënter en winstgevender fracken
Realistisch nieuw model wijst de weg naar efficiënter en winstgevender fracken
Hoofdlijnen
- Kunnen honden komkommers eten? Zijn ze veilig? Hun gezondheidsvoordelen uitgelegd
- Suiker in babyvoeding:waarom Nestlé rekening moet houden Afrika
- Wie kwam er met celtheorie?
- Wat zorgt ervoor dat vliegen aanvallen?
- Beoordeling van op SERS gebaseerde sensoren voor landbouwtoepassingen
- Wat zou er gebeuren als je levercellen in een hyptone oplossing zou stoppen?
- Soorten organismen die van plantencellen zijn gemaakt
- Nieuwe studie onderzoekt hoe het dengue-virus het gedrag van muggen verandert
- Wat is het voordeel van aseksuele reproductio?
- Nieuw polymeer kan de prestaties van organische en perovskiet-zonnecellen verbeteren

- Verdwijningshandeling:apparaat verdwijnt op commando na militaire missies

- Een verborgen elektronische overgang van S0 naar Tn in moleculen die zware atomen bevatten

- Techniek om transparante polyethyleenfilms zo sterk als aluminium te maken

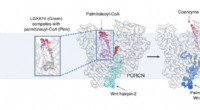
- Nieuwe cryo-EM-beelden werpen licht op Wnt-signalering
 Is rubber en glas 2 voorbeelden van kristallijne vaste stof?
Is rubber en glas 2 voorbeelden van kristallijne vaste stof?  Strontium nitraat- en natriumsulfide -participatiereacties?
Strontium nitraat- en natriumsulfide -participatiereacties?  De impact van de gebouwen van een stad op het weer meten
De impact van de gebouwen van een stad op het weer meten Het nauwkeurig bepalen van de energieniveaus van verschillende zonnematerialen voor hoogwaardige apparaten
Het nauwkeurig bepalen van de energieniveaus van verschillende zonnematerialen voor hoogwaardige apparaten Welke biologische moleculen worden gebruikt om energie op te slaan in levende organismen, variëren in structuur en vormen het grootste deel van het celmembraan?
Welke biologische moleculen worden gebruikt om energie op te slaan in levende organismen, variëren in structuur en vormen het grootste deel van het celmembraan?  Wat voor soort rots is Chainman Shale?
Wat voor soort rots is Chainman Shale?  Een eucharistie van zuurdesem of wafeltje? Wat een duizend jaar oude religieuze ruzie ons vertelt over gisting
Een eucharistie van zuurdesem of wafeltje? Wat een duizend jaar oude religieuze ruzie ons vertelt over gisting  Zijn alle brandstoffen voorbeelden van chemische energie?
Zijn alle brandstoffen voorbeelden van chemische energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

