
Wetenschap
Welke regel is het wanneer representatieve elementen bindingen vormen totdat ze acht elektronen in hun valance -schelpen hebben?
Hier is een uitsplitsing:
* Representatieve elementen: Dit zijn de elementen gevonden in groepen 1, 2 en 13-18 van het periodiek systeem.
* valentie -shell: De buitenste elektronenschil van een atoom.
* octetregel: Stelt dat atomen de neiging hebben om elektronen te winnen, verliezen of delen om een stabiele configuratie van acht elektronen in hun valentieschil te bereiken. Deze configuratie is vergelijkbaar met die van de edelgassen, die chemisch niet -reactief zijn.
Uitzonderingen op de octetregel:
* waterstof: Waterstof heeft slechts twee elektronen in zijn valentieschaal nodig om stabiel te zijn.
* elementen in de tweede periode: Elementen zoals boor en beryllium kunnen stabiel zijn met minder dan acht elektronen.
* elementen in periodes 3 en verder: Elementen zoals zwavel en fosfor kunnen soms meer dan acht elektronen in hun valentieschaal hebben vanwege de beschikbaarheid van lege D -orbitalen.
De Octet -regel is een nuttige richtlijn voor het begrijpen van chemische binding, maar het is belangrijk om te onthouden dat het geen strikte regel is en uitzonderingen heeft.
 Onderzoek toont aan wanneer de bevolkingsdruk toeneemt, voedsel wordt geïmporteerd
Onderzoek toont aan wanneer de bevolkingsdruk toeneemt, voedsel wordt geïmporteerd Cichlidenvissen uit het Afrikaanse Tanganyikameer werpen licht op hoe de diversiteit van organismen ontstaat
Cichlidenvissen uit het Afrikaanse Tanganyikameer werpen licht op hoe de diversiteit van organismen ontstaat  Ruimteradar suggereert Noord-Koreaanse kernbom gelijk aan 17 Hiroshimas
Ruimteradar suggereert Noord-Koreaanse kernbom gelijk aan 17 Hiroshimas Wat zijn de kenmerken van een tropische storm?
Wat zijn de kenmerken van een tropische storm?  Waarom werd orkaan Patricia zo snel een monster?
Waarom werd orkaan Patricia zo snel een monster?
Hoofdlijnen
- Draagt lichaamsbeweging ontwikkeling aan? Bij de zeeanemoon is de manier waarop je beweegt van belang
- Geometrie speelt een belangrijke rol in hoe cellen zich gedragen, onderzoekers rapporteren
- Onderzoek toont aan dat pesticiden generaties bijen kunnen beïnvloeden. Dit is wat je doet
- Wat zijn de verschillende soorten plantenaanpassingen?
- Kunnen celstructuren worden gezien onder lichtmicroscopen?
- UW-wetenschappers ontrafelen het mysterie van hoe griepvirussen zich vermenigvuldigen
- Rechtshandige gewoonte is misschien 2 miljoen jaar geleden begonnen
- Waarom gapen besmettelijk is bij bonobo's
- Waarom ademen mensen op de planeet Aarde?
- Onderzoek naar het creëren van zelfreinigende oppervlakken via 3D-printen

- De juiste formule voor het opschalen van de productie van veelbelovend materiaal om water te decontamineren

- Nieuwe synthese van complexe organische moleculen onthuld
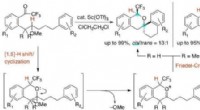
- Schimmelinfectie van het hoornvlies behandelen met synthetische moleculen

- Licht van een exotische kristalhalfgeleider kan leiden tot betere zonnecellen
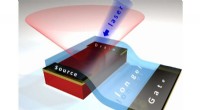
 Wat zijn enkele goede DNA-wetenschapsprojecten?
Wat zijn enkele goede DNA-wetenschapsprojecten?  Geeft de oostelijke rode knopboom schaduw?
Geeft de oostelijke rode knopboom schaduw?  Waarom wordt het natriumbenzoaat gemakkelijk geëxtraheerd in H20, terwijl het oorspronkelijke benzoëzuur geen H20 is?
Waarom wordt het natriumbenzoaat gemakkelijk geëxtraheerd in H20, terwijl het oorspronkelijke benzoëzuur geen H20 is?  De zon is magnetisch minder actief dan andere sterren
De zon is magnetisch minder actief dan andere sterren Wil je gezond eten en de planeet redden? Vervang rundvlees door Spirulina-algen, zeggen onderzoekers
Wil je gezond eten en de planeet redden? Vervang rundvlees door Spirulina-algen, zeggen onderzoekers  Bayer bevestigt voorspellingen terwijl de integratie van Monsanto vordert
Bayer bevestigt voorspellingen terwijl de integratie van Monsanto vordert Wat gebeurt er met het ecosysteem als een roofdiersoort extint is?
Wat gebeurt er met het ecosysteem als een roofdiersoort extint is?  Nieuw materiaal maakt koelapparaten energiezuiniger
Nieuw materiaal maakt koelapparaten energiezuiniger
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

