
Wetenschap
Hoe is kation gerelateerd aan het atoom?
* startpunt:het atoom
* Een atoom is de basiseenheid van een element. Het is elektrisch neutraal, wat betekent dat het een gelijk aantal protonen (positieve lading) en elektronen (negatieve lading) heeft.
* Een kation worden:elektronen verliezen
* Wanneer een atoom elektronen verliest, wordt het aantal protonen groter dan het aantal elektronen. Deze onbalans creëert een netto positieve lading.
* Het proces van het verliezen van elektronen wordt ionisatie genoemd .
Voorbeelden:
* natrium (na) :Een natriumatoom heeft 11 protonen en 11 elektronen. Wanneer het één elektron verliest, wordt het een natriumkation (Na+) met 11 protonen en 10 elektronen.
* calcium (ca) :Een calciumatoom heeft 20 protonen en 20 elektronen. Wanneer het twee elektronen verliest, wordt het een calciumkation (Ca2+) met 20 protonen en 18 elektronen.
Sleutelpunten:
* opladen: Het aantal verloren elektronen bepaalt de lading van het kation.
* stabiliteit: Atomen hebben de neiging elektronen te verliezen om een stabielere elektronenconfiguratie te bereiken, die vaak op een edelgas lijken.
* chemische binding: Kationen spelen een cruciale rol bij chemische binding, vooral in ionische verbindingen waar ze zich aangetrokken voelen tot anionen (negatief geladen ionen).
Samenvattend is een kation een positief geladen atoom (of molecuul) dat is gevormd door het verlies van een of meer elektronen. Het vertegenwoordigt een verandering in de lading- en elektronenconfiguratie van het atoom, wat leidt tot nieuwe chemische eigenschappen en interacties.
 Nieuwe dynamische sondes voor ionen die interageren met biomoleculen
Nieuwe dynamische sondes voor ionen die interageren met biomoleculen Hoe kalkwater wordt voorbereid in het laboratorium?
Hoe kalkwater wordt voorbereid in het laboratorium?  Wat zijn enkele items die gelijk zijn aan de Ozone vernietigen?
Wat zijn enkele items die gelijk zijn aan de Ozone vernietigen?  Als je een beker water kookt boven de bunsenbrander, wordt het dan gas?
Als je een beker water kookt boven de bunsenbrander, wordt het dan gas?  Handheld DNA-sequencers zijn veelbelovend voor het monitoren van microben tijdens voedselproductie
Handheld DNA-sequencers zijn veelbelovend voor het monitoren van microben tijdens voedselproductie
 Welke levende dingen moeten hun voedsel opnemen of absorberen en kunnen geen voedsel intern maken?
Welke levende dingen moeten hun voedsel opnemen of absorberen en kunnen geen voedsel intern maken?  NASA ziet Wilfred degenereren tot een trog
NASA ziet Wilfred degenereren tot een trog Verse zeespray wordt zuur na in de lucht te zijn geweest
Verse zeespray wordt zuur na in de lucht te zijn geweest Verhaal van twee klimaatcrises geeft aanwijzingen voor het heden
Verhaal van twee klimaatcrises geeft aanwijzingen voor het heden Klimaatverandering leidt tot ongekende bosbranden
Klimaatverandering leidt tot ongekende bosbranden
Hoofdlijnen
- DropSynth, een eenpotsbenadering van gensynthese
- Wat is een kenmerk dat doorgaans niet wordt gebruikt om biomen te classificeren?
- Hoe wordt de wetenschap gebruikt in de landbouw?
- Wat is een voorbeeld van een presynaptische cel?
- Facilitated Diffusion: Definition, Example & Factors
- Chinese wetenschappers onthullen een nieuwe signaalroute voor koude tolerantie in rijst
- Waarom is water belangrijk voor het uitscheidingssysteem in het lichaam?
- Uitsterven dreigt voor twee zeldzame vogelsoorten na verwoestende orkanen
- Onderzoekers onthullen het mechanisme waarmee cellulaire kernen hun positie in spiercellen bereiken
- Wetenschappers verbeteren kleur en textuur van kweekvlees

- Miniatuurdruppels kunnen een raadsel over de oorsprong van het leven oplossen

- Veenbessen kunnen darmgezondheidsproblemen voor vleeseters verminderen

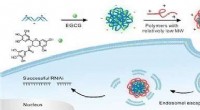
- Groene theeverbinding helpt siRNA in cellen te glippen
- Oorzaak van kathodedegradatie geïdentificeerd voor nikkelrijke materialen

 Waarom wordt ether gebruikt als extractiemiddel?
Waarom wordt ether gebruikt als extractiemiddel?  Wetenschappers ontwikkelen een statistische oplossing voor het dateringsprobleem van archeologie
Wetenschappers ontwikkelen een statistische oplossing voor het dateringsprobleem van archeologie Amazon Go-winkels accepteren contant geld onder toenemende druk om kopers met een laag inkomen te bedienen
Amazon Go-winkels accepteren contant geld onder toenemende druk om kopers met een laag inkomen te bedienen Wat is de belangrijkste vegetatie van Corpus Christi Texas?
Wat is de belangrijkste vegetatie van Corpus Christi Texas?  Waar zal Amazon zijn tweede hoofdkantoor vestigen? Wat je moet weten
Waar zal Amazon zijn tweede hoofdkantoor vestigen? Wat je moet weten Is ammoniumchloride ionisch of covalent?
Is ammoniumchloride ionisch of covalent?  Geen ruimte voor groenten? Pot je planten op
Geen ruimte voor groenten? Pot je planten op Wat is het verschil tussen radiale energie en tangentiële energie?
Wat is het verschil tussen radiale energie en tangentiële energie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

