
Wetenschap
Waarom is het onwaarschijnlijk dat calciumchloridekristallen zijn gemaakt van metaal?
* ionische binding: Calciumchloride (CaCl₂) wordt gevormd door ionische binding. Dit betekent dat calcium (Ca), een metaal, twee elektronen verliest om een positief geladen ion te worden (ca²⁺). Chloor (CL), een niet -metaal, krijgt elk één elektron om negatief geladen ionen te worden (CL⁻). Deze tegengesteld geladen ionen trekken elkaar sterk aan en vormen de ionische compound CaCl₂.
* kristalstructuur: De sterke elektrostatische aantrekkingskracht tussen de ionen leidt tot een sterk georganiseerde, herhaalde opstelling van ionen die een kristalrooster worden genoemd. Dit is de reden waarom calciumchloride kristallen vormt.
* Eigenschappen van metalen: Metalen zijn meestal glanzend, kneedbaar, ductiele en goede geleiders van warmte en elektriciteit. Calciumchloride -kristallen vertonen deze eigenschappen niet.
Samenvattend: De aard van ionische binding in calciumchloride en de resulterende kristalstructuur verschilt fundamenteel van de eigenschappen en structuur van metalen. Daarom is het onwaarschijnlijk dat calciumchloridekristallen zijn gemaakt van metaal.
 Wat is een voorbeeld van cyclische koolwaterstof?
Wat is een voorbeeld van cyclische koolwaterstof?  Tijdens een reactie wordt de OH -groep van een alcohol vervangen door chlooratoom. Welk type gebeurde?
Tijdens een reactie wordt de OH -groep van een alcohol vervangen door chlooratoom. Welk type gebeurde?  Elementen in planten gebruiken om de efficiëntie van de brandstofcel te verhogen en tegelijkertijd de kosten te verlagen
Elementen in planten gebruiken om de efficiëntie van de brandstofcel te verhogen en tegelijkertijd de kosten te verlagen Domino-achtige kristallisatie van glas
Domino-achtige kristallisatie van glas Hechtgedrag van zelfconstructieve materialen voor het eerst gemeten
Hechtgedrag van zelfconstructieve materialen voor het eerst gemeten
 Waarom is slechts een klein percentage van het zoete water op aarde voor ons beschikbaar?
Waarom is slechts een klein percentage van het zoete water op aarde voor ons beschikbaar?  Hoe Cactus -bladeren werken?
Hoe Cactus -bladeren werken?  Waarom klimaatverandering parasitaire ziekten moeilijker te voorspellen maakt
Waarom klimaatverandering parasitaire ziekten moeilijker te voorspellen maakt  Bepalen wanneer mensen de planeet op grote schaal begonnen te beïnvloeden
Bepalen wanneer mensen de planeet op grote schaal begonnen te beïnvloeden Nieuwe radaranalysemethode kan de rivierveiligheid in de winter verbeteren
Nieuwe radaranalysemethode kan de rivierveiligheid in de winter verbeteren
Hoofdlijnen
- Onderzoeken waarom mannetjes groter zijn dan vrouwtjes onder zoogdieren
- Waarom hebben de meeste mensen 23 paar chromosomen?
- Zijn alle dieren eencellig en hebben eukaryotische cellen?
- Hoe leven met roofdieren inheemse soorten kan helpen overleven
- Nieuw onderzoek laat zien hoe pathogene E. coli O157:H7 zich bindt aan verse groenten
- Hoe de gedachten van een kwal te lezen
- Wat zijn de eerste stappen die wetenschappers nemen om de oorzaak van een ziekte te analyseren?
- Hoe bevoordeelt natuurlijke selectie een erfelijke eigenschap?
- Organismen met aanpassingen om te strijden om beperkte middelen kunnen overleven en hun genen nakomelingen doorgeven?
- Chemici ontwikkelen een nieuw milieuvriendelijk materiaal voor afvalwaterzuivering

- Geldruppels voor regeneratieve geneeskunde
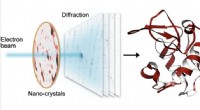
- Besluipen op kleine kristallen met elektronendiffractie
- Mechanische ingenieurs ontwikkelen proces om piëzo-elektrische materialen in 3D te printen

- Ontdekking van een nieuw fenomeen, een game-changer voor efficiënte bioproductie van nuttige chemicaliën
 Waar de Hawaiiaanse eilanden gevormd door aardbevingen of vulkanen?
Waar de Hawaiiaanse eilanden gevormd door aardbevingen of vulkanen?  Abnormale geleidbaarheid in gedraaid dubbellaags grafeen met een lage hoek
Abnormale geleidbaarheid in gedraaid dubbellaags grafeen met een lage hoek Nieuw onderzoek laat zien hoe onderzees grondwater de groei van koraalriffen beïnvloedt
Nieuw onderzoek laat zien hoe onderzees grondwater de groei van koraalriffen beïnvloedt  Werknemers die lange dagen maken, hebben plezier in hun werk, maar degenen die dat niet doen, geven snel op
Werknemers die lange dagen maken, hebben plezier in hun werk, maar degenen die dat niet doen, geven snel op Wat is de breedtegraad en lengtegraad van Port Alberni BC?
Wat is de breedtegraad en lengtegraad van Port Alberni BC?  Verschil tussen waterdruk en luchtdruk
Verschil tussen waterdruk en luchtdruk  Wat zijn de drie tijdsperioden waarin de dinosaurussen leefden?
Wat zijn de drie tijdsperioden waarin de dinosaurussen leefden?  Welke landen zijn onder de tropic van Capricor?
Welke landen zijn onder de tropic van Capricor?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

