
Wetenschap
Hoe beïnvloedt zout het smelt- en vriespunt van water?
Het vriespunt verlagen (depressie van het vriespunt):
* Verstoring van de waterstructuur: Wanneer zout (NaCl) oplost in water, breekt het af in natrium (Na+) en chloride (Cl-) ionen. Deze ionen verstoren de normale waterstofbinding tussen watermoleculen. Watermoleculen vormen normaal gesproken een gestructureerd, kristallijn rooster bij het bevriezen. De ionen interfereren met deze formatie, waardoor het voor het water moeilijker is om te stollen.
* Meer energie nodig: Als gevolg hiervan moet het water kouder zijn dan 0 ° C (32 ° F) om te bevriezen. Dit temperatuurverschil wordt het vriespuntdepressie genoemd.
* Het bedrag is belangrijk: Hoe meer zout je oplost, hoe groter het vriespuntdepressie.
Het smeltpunt verhogen (kookpunthoogte):
* Vergelijkbaar mechanisme: Hetzelfde principe dat het vriespunt verlaagt, is ook van toepassing op het kookpunt. De opgeloste ionen verstoren de waterstructuur en maken het moeilijker voor de watermoleculen om te ontsnappen in de dampfase.
* Hogere temperatuur nodig: Als gevolg hiervan moet het water heter zijn dan 100 ° C (212 ° F) om te koken.
Waarom is dit belangrijk?
* Road De-icing: Zout wordt gebruikt om ijs en sneeuw op wegen in de winter te smelten omdat het het vriespunt van water verlaagt. Dit voorkomt de vorming van een solide ijslaag, waardoor wegen veiliger worden om te rijden.
* Voedselbehoud: Zout wordt gebruikt om voedsel te behouden omdat het het vriespunt van het water in het voedsel verlaagt, waardoor het voor bacteriën moeilijker is om te groeien.
* Andere toepassingen: Bevriezende puntdepressie en kookpunthoogte hebben toepassingen in veel andere gebieden, waaronder:
* antivries voor motoren: Antivries bevat verbindingen die het vriespunt van de koelvloeistof verlagen, waardoor het niet kan bevriezen bij koud weer.
* Saltwateroplossingen: Zoutwater heeft een lager vriespunt en een hoger kookpunt dan zoet water, daarom bevriezen de oceanen niet vast in de winter.
Laat het me weten als je nog andere vragen hebt over zout en de effecten ervan op water!
 Wetenschappers leggen de basis voor een betrouwbare marihuana-ademtester
Wetenschappers leggen de basis voor een betrouwbare marihuana-ademtester 3D-geprinte kunstmatige hoornvliezen vergelijkbaar met menselijke hoornvliezen
3D-geprinte kunstmatige hoornvliezen vergelijkbaar met menselijke hoornvliezen Wat zijn stoffen die uit ruwe olie zijn geëxtraheerd zonder te worden veranderd?
Wat zijn stoffen die uit ruwe olie zijn geëxtraheerd zonder te worden veranderd?  Onder welke omstandigheden leiden metalloïden warmte en elektriciteit?
Onder welke omstandigheden leiden metalloïden warmte en elektriciteit?  Hoe verhoogt het gebruik van synthetische producten zoals plastic de fossiele brandstoffen?
Hoe verhoogt het gebruik van synthetische producten zoals plastic de fossiele brandstoffen?
 Hoe bruine ratten van schepen kropen en Noord-Amerikaanse steden veroverden
Hoe bruine ratten van schepen kropen en Noord-Amerikaanse steden veroverden  Californië zingt in de regen
Californië zingt in de regen Harde rotsen uit de Himalaya verhogen het overstromingsrisico voor miljoenen
Harde rotsen uit de Himalaya verhogen het overstromingsrisico voor miljoenen Het magnetische veld van de aarde staat niet op het punt om te keren, studie vondsten
Het magnetische veld van de aarde staat niet op het punt om te keren, studie vondsten Trump stelt besluit over klimaatakkoord Parijs uit
Trump stelt besluit over klimaatakkoord Parijs uit
Hoofdlijnen
- Hoe beïnvloedt het sociale gedrag van tarweplanten de graanproductie?
- Wetenschappers hebben ontdekt dat de micro-inkapselingstechniek de efficiëntie van theeboomolie verhoogt voor duurzame toepassingen
- Hoe de hoed past:onderzoek naar structurele biologie onthult de vorm van het epigenetische enzymcomplex
- Wat zijn alle mogelijke doelen waarvoor een groeiende zaailing voedsel kan gebruiken die in zijn zaadlobben is opgeslagen?
- IU-informatici laten nieuwe niveaus van verfijning zien in het voorspellen van menselijke mobiliteit en verspreiding van epidemieën
- Wetenschappers ontdekken nieuwe uitgestorven mierensoorten ingekapseld in barnsteen
- Hoe worden genen aan- en uitgezet?
- Waarom levert een gebrek aan overgangsvormen problemen op voor de evolutionaire hypothese?
- Genetische studie onderzoekt manieren om de productiviteit en malsheid van vlees te verhogen
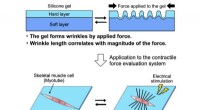
- Wetenschappers ontwikkelen directe meting voor kracht van skeletspiermyotubes
- Schimmelinfectie van het hoornvlies behandelen met synthetische moleculen

- Wanneer chemie met groen licht nabootst wat er in het leven gebeurt

- Fluorescerend kristal mysterie opgelost
- Geneesmiddelenscreening op de chip voor het identificeren van antibiotica-interacties in acht uur

 Is hun geen limiet in hoe groot of klein een cel kan zijn?
Is hun geen limiet in hoe groot of klein een cel kan zijn?  Hoe een zeshoek op te lossen
Hoe een zeshoek op te lossen  Drie aanpassingen voor een dolfijn
Drie aanpassingen voor een dolfijn Welke drie stoffen worden normaal gesproken in bloed aangetroffen, maar niet in urine?
Welke drie stoffen worden normaal gesproken in bloed aangetroffen, maar niet in urine?  Hoe ziet versteende hout eruit?
Hoe ziet versteende hout eruit?  Welk deel van een plantencel verzamelt lichtenergie?
Welk deel van een plantencel verzamelt lichtenergie?  Wat voor soort zuur is HIO 2?
Wat voor soort zuur is HIO 2?  Het is tijd om het verstoorde Amerikaanse voedselsysteem van de grond af aan te heroverwegen
Het is tijd om het verstoorde Amerikaanse voedselsysteem van de grond af aan te heroverwegen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

