
Wetenschap
Wat is de elektronenconfiguratie van fosfor (P)?
1S² 2S² 2P⁶ 3S² 3P³
Hier is hoe je het kunt begrijpen:
* 1S²: Het eerste energieniveau (n =1) heeft één subshell (s) met 2 elektronen.
* 2S²: Het tweede energieniveau (n =2) heeft één subshell (s) met 2 elektronen.
* 2p⁶: Het tweede energieniveau (n =2) heeft één subshell (P) met 6 elektronen.
* 3S²: Het derde energieniveau (n =3) heeft één subshell (s) met 2 elektronen.
* 3p³: Het derde energieniveau (n =3) heeft één subshell (P) met 3 elektronen.
Verklaring:
* Fosfor heeft een atoomnummer van 15, wat betekent dat het 15 protonen en 15 elektronen heeft.
* We vullen de orbitalen in volgorde van toenemende energieniveaus, volgens het AUFBAU -principe.
* De S -subshell kan maximaal 2 elektronen bevatten en de P -subshell kan maximaal 6 elektronen bevatten.
* De 3P -subshell heeft slechts 3 elektronen in fosfor, waardoor 3 lege ruimtes achterblijven. Dit is de reden waarom fosfor zeer reactief is en de neiging heeft om 3 elektronen te krijgen om een stabiel octet te bereiken.
 NASA vangt ontwikkeling van tropische cycloon Nuri in Zuid-Chinese Zee
NASA vangt ontwikkeling van tropische cycloon Nuri in Zuid-Chinese Zee Overstromingen langs de kust versterken de ophoping van methaan in bossen
Overstromingen langs de kust versterken de ophoping van methaan in bossen Top EPA-adviseurs dagen al lang bestaande luchtvervuilingswetenschap uit, een bedreiging voor de gezondheid van de Amerikanen
Top EPA-adviseurs dagen al lang bestaande luchtvervuilingswetenschap uit, een bedreiging voor de gezondheid van de Amerikanen Grond- en satellietobservaties brengen schade aan gebouwen in kaart na de explosie in Beiroet
Grond- en satellietobservaties brengen schade aan gebouwen in kaart na de explosie in Beiroet Welke invloed hebben lokale droge meren op de luchtkwaliteit en de menselijke gezondheid?
Welke invloed hebben lokale droge meren op de luchtkwaliteit en de menselijke gezondheid?
Hoofdlijnen
- Wat is een micro-oranisme?
- Verrassend snelle evolutie waargenomen bij hagedissoorten
- Waarom walvissen geen hersenbeschadiging oplopen als ze zwemmen
- Centriole: definitie, functie en structuur
- Wat zijn de intermoleculaire krachten van HClO?
- Evolueren dieren nog steeds?
- Kan slapen me gelukkig maken?
- Wat doet een celmembraan in wortelhaarcel?
- Seizoensgedrag bij planten en dieren wordt gestimuleerd door?
- Het minimaliseren van brandstofexplosies en branden door ongelukken en terroristische daden met polymeren

- Iridium en 2-methylfenantroline versnellen katalytische boryleringsreacties

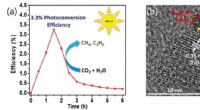
- Een-twee-stempel katalysatoren die koolstofdioxide opvangen voor schonere brandstoffen
- Stal, zelfverstorende microbellen als intraveneuze zuurstofdragers

- De meeste eiwitinformatie ooit vastgelegd in een enkele cel dankzij nieuwe nanoPOTS-technologie

 Stonehenge stond mogelijk zowel op één lijn met de maan als met de zon
Stonehenge stond mogelijk zowel op één lijn met de maan als met de zon  Wat is een drone?
Wat is een drone?  Wat is een spin-off van de ruimte?
Wat is een spin-off van de ruimte?  Wat zijn kenmerken van enzymen?
Wat zijn kenmerken van enzymen?  Vroege ziektediagnose kan drastisch worden verbeterd met nieuw detectiesysteem
Vroege ziektediagnose kan drastisch worden verbeterd met nieuw detectiesysteem Een lichtstraal kan worden gezien als het door A paste?
Een lichtstraal kan worden gezien als het door A paste?  Hoe desinformatie te bestrijden in het post-waarheidstijdperk
Hoe desinformatie te bestrijden in het post-waarheidstijdperk  Meer controle krijgen over brandstofcelmembranen
Meer controle krijgen over brandstofcelmembranen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

