
Wetenschap
Bepaalt het elektron de reactiviteit van een atoom?
elektronen en reactiviteit:
* valentie -elektronen: De elektronen in de buitenste schaal (valentieschaal) zijn degenen die betrokken zijn bij chemische binding. Dit zijn degenen die bepalen hoe een atoom zal omgaan met andere atomen.
* Elektronenconfiguratie: De specifieke opstelling van elektronen in de schalen en subshells van een atoom (elektronenconfiguratie) beïnvloedt zijn reactiviteit. Atomen met een volledige valentie -schaal (zoals nobele gassen) zijn zeer stabiel en niet -reactief. Atomen met een of enkele ontbrekende elektronen in hun valentieschaal zijn meestal zeer reactief.
* elektronegativiteit: Deze eigenschap weerspiegelt hoe sterk een atoom elektronen in een binding aantrekt. Sterk elektronegatieve atomen zijn meestal reactiever, omdat ze eerder elektronen krijgen en anionen vormen.
Andere factoren die de reactiviteit beïnvloeden:
* Nucleaire lading: Het aantal protonen in de kern beïnvloedt de aantrekkingskracht voor elektronen. Een hogere nucleaire lading leidt in het algemeen tot een sterkere aantrekkingskracht voor elektronen, waardoor het atoom reactiever wordt.
* Atomaire maat: Kleinere atomen zijn meestal reactiever, omdat hun valentie -elektronen dichter bij de kern zijn en gemakkelijker toegankelijk zijn voor binding.
Samenvattend:
De rol van het elektron in reactiviteit is complex en veelzijdig. Het is niet alleen het elektron zelf, maar de configuratie, de elektronegativiteit van het atoom en andere factoren die uiteindelijk bepalen hoe reactief een atoom zal zijn.
 Is het leven op waterbasis ontstaan zonder water?
Is het leven op waterbasis ontstaan zonder water?  Pieken in koolstofemissies gedetecteerd met NASA-satelliet
Pieken in koolstofemissies gedetecteerd met NASA-satelliet Klimaatrapport:VS getroffen door meer dan 100 tornado's, zware sneeuwval in april
Klimaatrapport:VS getroffen door meer dan 100 tornado's, zware sneeuwval in april  17% van de voedselproductie wereldwijd wordt verspild, VN-rapport schattingen
17% van de voedselproductie wereldwijd wordt verspild, VN-rapport schattingen Aeolus werpt licht op polaire vortex
Aeolus werpt licht op polaire vortex
Hoofdlijnen
- Hoe je je handen kunt wassen om sperma te doden
- De krimpende eland van Isle Royale
- Wat is de studie van functie in een biologisch organisme?
- Wat is de moleculaire structuur van een appel?
- Hoe ‘extracellulaire chaperonnes’ abnormale eiwitten helpen verwijderen
- Hoe neemt een slijmvorm beslissingen zonder hersenen?
- EU stemt ermee in om in 2018 meer vis op een duurzame manier te vangen
- Hoe grassen inteelt vermijden
- Hoeveel calorieën verbrand ik als ik lach?
- Anti-verouderingsmolecuul NAD+ krijgt een boost door het blokkeren van een enzym
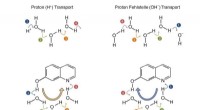
- Vooruit of achteruit? Nieuwe routes voor protonen in water of methanol
- Nieuwe methode om mineralen te analyseren onder terrestrische en Martiaanse atmosferische omstandigheden

- Alle prestaties, geen gedoe:nitrilhydrogenering goed gedaan

- Een nieuwe manier om de cel binnen te gaan met behulp van superchaotrope eigenschappen van boorclusters
 De bio-economie:duurzame groene groei realiseren?
De bio-economie:duurzame groene groei realiseren?  Waarom heeft het Internationale Ruimtestation zonnepanelen nodig?
Waarom heeft het Internationale Ruimtestation zonnepanelen nodig?  Het echte Paleodieet:nieuw archeologisch bewijs verandert onze mening over hoe oude mensen voedsel bereidden
Het echte Paleodieet:nieuw archeologisch bewijs verandert onze mening over hoe oude mensen voedsel bereidden  NASA's NavCube zou een demonstratie van röntgencommunicatie in de ruimte kunnen ondersteunen - een primeur voor NASA
NASA's NavCube zou een demonstratie van röntgencommunicatie in de ruimte kunnen ondersteunen - een primeur voor NASA Wat wordt bedoeld met de raaklijnwet in de natuurkunde?
Wat wordt bedoeld met de raaklijnwet in de natuurkunde?  Wat is de oplosbaarheid van motorolie?
Wat is de oplosbaarheid van motorolie?  De korte, tumultueus beroepsleven van een Major League Baseball-werper
De korte, tumultueus beroepsleven van een Major League Baseball-werper Het bedekken van metalen katalysatoroppervlakken met dunne tweedimensionale oxidematerialen kan chemische reacties versterken
Het bedekken van metalen katalysatoroppervlakken met dunne tweedimensionale oxidematerialen kan chemische reacties versterken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

