
Wetenschap
Hoe vindt u de valentie van chloor natrium en magnesium?
Valentie begrijpen
Valentie verwijst naar de combinerende kracht van een element. Het is het aantal elektronen dat een atoom moet winnen, verliezen of delen om een stabiele elektronenconfiguratie te bereiken (meestal als een edelgas).
1. Chloor (CL)
* Elektronenconfiguratie: Chloor heeft 17 elektronen, met een elektronische configuratie van 2, 8, 7.
* Stabiele configuratie: Chloor heeft nog een elektron nodig om een stabiel octet (8 elektronen) te bereiken in de buitenste schaal zoals argon (AR).
* Valentie: Daarom heeft chloor een valentie van 1 .
2. Natrium (NA)
* Elektronenconfiguratie: Natrium heeft 11 elektronen, met een elektronische configuratie van 2, 8, 1.
* Stabiele configuratie: Natrium kan gemakkelijk zijn buitenste elektron verliezen om een stabiele configuratie zoals neon (NE) te bereiken.
* Valentie: Natrium heeft een valentie van 1 .
3. Magnesium (mg)
* Elektronenconfiguratie: Magnesium heeft 12 elektronen, met een elektronische configuratie van 2, 8, 2.
* Stabiele configuratie: Magnesium kan zijn twee buitenste elektronen verliezen om een stabiele configuratie zoals neon (NE) te bereiken.
* Valentie: Magnesium heeft een valentie van 2 .
Key Points
* metalen: Metalen verliezen meestal elektronen om een stabiele configuratie te bereiken, wat resulteert in positieve ionen. Hun valentie wordt weergegeven door een positief getal.
* niet -metalen: Niet -metalen krijgen meestal elektronen om een stabiele configuratie te bereiken, wat resulteert in negatieve ionen. Hun valentie wordt weergegeven door een negatief getal.
* Valentie en chemische binding: Valentie speelt een cruciale rol bij chemische binding. Atomen met complementaire valenties (bijv. Natrium met valentie 1 en chloor met valentie 1) kunnen gemakkelijk ionische bindingen vormen.
Laat het me weten als je de valentie van andere elementen wilt verkennen!
 Welke soorten werden geoxideerd of gereduceerd in HCl?
Welke soorten werden geoxideerd of gereduceerd in HCl?  Microschaal thermoforese om hits van high-throughput screening te karakteriseren
Microschaal thermoforese om hits van high-throughput screening te karakteriseren Kan er een covalente binding ontstaan wanneer elektronen worden overgedragen tussen 2 atomen?
Kan er een covalente binding ontstaan wanneer elektronen worden overgedragen tussen 2 atomen?  Nieuwe benadering voorspelt het altijd evoluerende gedrag van glas bij verschillende temperaturen
Nieuwe benadering voorspelt het altijd evoluerende gedrag van glas bij verschillende temperaturen Wat zijn enkele kenmerken van polymeren?
Wat zijn enkele kenmerken van polymeren?
 De stroom van de Fitzroy-rivier in West-Australië is cruciaal voor het overleven van bedreigde zaagvissen
De stroom van de Fitzroy-rivier in West-Australië is cruciaal voor het overleven van bedreigde zaagvissen Het verband tussen stikstofbenutting en grondwaterkwaliteit is duidelijk
Het verband tussen stikstofbenutting en grondwaterkwaliteit is duidelijk Everest-redders halen lichamen van twee Indiase klimmers op
Everest-redders halen lichamen van twee Indiase klimmers op Hoe vermijden trekvogels roofdieren tijdens het tanken?
Hoe vermijden trekvogels roofdieren tijdens het tanken?  Hoe de Australische mierendoderspin mieren vangt
Hoe de Australische mierendoderspin mieren vangt
Hoofdlijnen
- Onderzoekers vinden neuronale paden bij ratten die sociale verzorging stimuleren
- Onderzoek verklaart waarom hennep en marihuana verschillend zijn
- Meer dan honderd grienden die aan de westkust van Australië zijn gestrand, zijn gered, zegt de onderzoeker
- Nieuwe ondersoort van Begonia gemeld uit Filipijnen
- Wordt uw Facebook-account het doelwit van voedingsbedrijven?
- Welke kenmerken gebruikte Carolus Linnaeus om organismen in groepen en subgroepen te plaatsen?
- Onderzoekers krijgen voor het eerst een volledig beeld van eiwit achter tastzin
- Hoe minder eten in het vroege leven zou kunnen helpen bij de voortplanting later
- Waarom werden archaea en bacteriën tot voor kort gegroepeerd door biologen?
- Wetenschappers onthullen routekaart om de ontwikkeling van osteoporosebehandeling te ondersteunen

- Veelzijdige nieuwe materiaalfamilie kan realistische protheses bouwen, futuristische legerplatforms

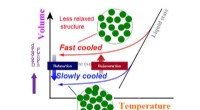
- Op maat gemaakte verharding van bulkmetaalglas veroorzaakt door 2-D gradiëntverjonging
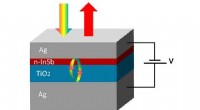
- Onderzoekers komen op de golflengte van de consument met InSb-technologie
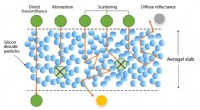
- Aerogels voor zonne-apparaten en ramen
 IJsberg van biljoen ton breekt Antarctica af (update)
IJsberg van biljoen ton breekt Antarctica af (update) Streaming tv-diensten:wat ze kosten, wat je krijgt
Streaming tv-diensten:wat ze kosten, wat je krijgt  Vereenvoudiging van kwantuminteracties op lange afstand in systemen met veel lichamen
Vereenvoudiging van kwantuminteracties op lange afstand in systemen met veel lichamen Onderzoek onthult bewijs van geweld in een tijd van crisis in het oude Peru
Onderzoek onthult bewijs van geweld in een tijd van crisis in het oude Peru  Wat is aanpassing van de citroenboom?
Wat is aanpassing van de citroenboom?  Wat is waar over stikstof en zuurstof?
Wat is waar over stikstof en zuurstof?  Wat voor soort cel wordt gevormd als chromosomen van een sperma -oproep en een eiermoeken?
Wat voor soort cel wordt gevormd als chromosomen van een sperma -oproep en een eiermoeken?  NASA-missie zal de kosmos bestuderen met een stratosferische ballon
NASA-missie zal de kosmos bestuderen met een stratosferische ballon
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

