
Wetenschap
Waarom wordt zout verspreid op bevroren oppervlak?
Hier is hoe het werkt:
1. zout lost op in water: Wanneer zout (natriumchloride) op ijs wordt bestrooid, lost het op in de dunne laag water die zich natuurlijk op het ijsoppervlak vormt.
2. ionen verstoren watermoleculen: Het opgeloste zout breekt af in ionen (natrium en chloride). Deze ionen interfereren met de vorming van de normale, kristallijne structuur die ijs moet bevroren blijven.
3. Lager vriespunt: Deze verstoring maakt het voor watermoleculen moeilijker om te bevriezen, waardoor het vriespunt van het water effectief wordt verlaagd.
4. het ijs smelten: Naarmate het vriespunt wordt verlaagd, begint het ijs te smelten, zelfs als de temperatuur onder 32 ° F (0 ° C) is.
Kortom, zout doet het ijs smelten door het vriespunt van water te laten zakken. Dit proces helpt om wegen en trottoirs veiliger te maken door het ijs te verwijderen en een minder glad oppervlak te creëren.
 Waarom werd de perspectieftechniek in deze periode niet als mooi beschouwd?
Waarom werd de perspectieftechniek in deze periode niet als mooi beschouwd?  Landen met de hoogste sterfte door vervuiling, sterftecijfers
Landen met de hoogste sterfte door vervuiling, sterftecijfers Wetlands van New York City zijn mogelijk onwetende generator van broeikasgassen
Wetlands van New York City zijn mogelijk onwetende generator van broeikasgassen Overstromingsgevoelige populaties met bijna 25% gestegen sinds 2000:studie
Overstromingsgevoelige populaties met bijna 25% gestegen sinds 2000:studie Amerikaans klimaatbesluit laat Europa verbolgen achter, verbijsterd
Amerikaans klimaatbesluit laat Europa verbolgen achter, verbijsterd
Hoofdlijnen
- Virusstamping - een veelzijdige nieuwe methode voor genetische manipulatie van afzonderlijke cellen
- Het Y-chromosoom verdwijnt – dus wat zal er met mannen gebeuren?
- Wat zijn de verschillen van eenvoudig en gestratificeerd weefsel?
- Hoe vitamines, steroïden en mogelijke antivirale middelen SARS-CoV-2 kunnen beïnvloeden
- Onderzoekers ontdekken nieuwe functie van oncoproteïnen
- Studie werpt nieuw licht op hoe dieren en planten reageren op veranderingen in de omgeving
- Hoe massale uitstervingen de evolutie van dinosauriërs aandreven
- Onderzoekers ontdekken de sleutel tot het moleculaire mysterie van hoe planten reageren op veranderende omstandigheden
- Wil je de bijen redden? Let op ziekteverwekkers en bloemen
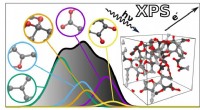
- Een model dat is getraind om spectroscopische profielen te voorspellen, helpt de structuur van materialen te ontcijferen
- Studie vindt fluor als mogelijke vervanging voor lithium in oplaadbare batterijen
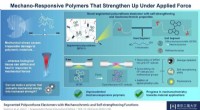
- Nieuw polymeer wordt harder en verandert van kleur bij mechanische belasting
- Een zelfherstellend composiet

- Nieuw gesynthetiseerde AM-III-koolstof is tot nu toe het hardste en sterkste amorfe materiaal

 Het samenvoegen van antenne en elektronica verhoogt de energie- en spectrumefficiëntie
Het samenvoegen van antenne en elektronica verhoogt de energie- en spectrumefficiëntie Hoe Finland omarmde om ‘de gelukkigste natie ter wereld’ te zijn
Hoe Finland omarmde om ‘de gelukkigste natie ter wereld’ te zijn  Wip van Indo-Pacific zomermoessons veroorzaakt door de tropische Atlantische Oceaan
Wip van Indo-Pacific zomermoessons veroorzaakt door de tropische Atlantische Oceaan Heeft donderen of bliksem invloed op apparaten zoals computer?
Heeft donderen of bliksem invloed op apparaten zoals computer?  Sabeltandtijgerskelet wordt verkocht voor meer dan $ 84, 000
Sabeltandtijgerskelet wordt verkocht voor meer dan $ 84, 000 Hoe liften werken
Hoe liften werken  Ruimtewandelende astronaut gaat om met gerafelde ketting, slechte jetpack (update)
Ruimtewandelende astronaut gaat om met gerafelde ketting, slechte jetpack (update) HBO Max wordt duurder dan Netflix, Disney of Apple. Betekent dit dat het een moeilijke verkoop zal zijn?
HBO Max wordt duurder dan Netflix, Disney of Apple. Betekent dit dat het een moeilijke verkoop zal zijn?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

