
Wetenschap
Hoeveel mol mangaan bevindt zich in 0 punt 1 gehydrateerd II sulfaat MnSO4 4H2O met een RFM 223?
1. Bepaal de molaire massa van mangaan (Mn):
* De molaire massa van Mn is ongeveer 54,94 g/mol.
2. Bereken de mol mangaan in 0,1 g van het gehydrateerde zout:
* Stap 1:Zoek het massapercentage van Mn in het gehydrateerde zout:
* Molaire massa van mnso₄ · 4h₂o =223 g/mol (gegeven)
* Massapercentage van Mn =(molaire massa van Mn / molaire massa van mnso₄ · 4h₂o) * 100%
* Massapercentage van Mn =(54,94 g/mol/223 g/mol) * 100% ≈ 24,6%
* Stap 2:Bereken de massa Mn in 0,1 g van het gehydrateerde zout:
* Massa van Mn =0,1 g * 24,6% =0,0246 g
* Stap 3:Bereken de mol Mn:
* Mol Mn =massa Mn / molaire massa van Mn
* Mol Mn =0,0246 g/54,94 g/mol ≈ 0,000448 mol
Daarom is ongeveer 0,000448 mol mangaan opgenomen in 0,1 g mnso₄ · 4h₂o.
 Kunnen defecten inerte materialen omzetten in bruikbare, actieve materialen?
Kunnen defecten inerte materialen omzetten in bruikbare, actieve materialen?  Fysieke en chemische eigenschappen van natriumbicarbonaat
Fysieke en chemische eigenschappen van natriumbicarbonaat Waarom beïnvloedt suiker het vriespunt van water?
Waarom beïnvloedt suiker het vriespunt van water?  Hoe maak je Pure Capsaicin
Hoe maak je Pure Capsaicin  Materiaalonderzoek onderzoekt ontwerpregels en synthese van kandidaten voor kwantumgeheugen
Materiaalonderzoek onderzoekt ontwerpregels en synthese van kandidaten voor kwantumgeheugen
 Waar werd goud gevonden in de natuur?
Waar werd goud gevonden in de natuur?  Deconcentratie is nodig om de emissies te verminderen en de overgang naar schone energiebronnen, vondsten melden
Deconcentratie is nodig om de emissies te verminderen en de overgang naar schone energiebronnen, vondsten melden Stadsland zou groenten en fruit kunnen verbouwen voor 15 procent van de bevolking, uit onderzoek blijkt
Stadsland zou groenten en fruit kunnen verbouwen voor 15 procent van de bevolking, uit onderzoek blijkt Met plastic gevulde maag van Thaise schildpadden benadrukt oceaancrisis
Met plastic gevulde maag van Thaise schildpadden benadrukt oceaancrisis Kunnen veranderende sociale normen de klimaatverandering helpen verzachten?
Kunnen veranderende sociale normen de klimaatverandering helpen verzachten?
Hoofdlijnen
- Waarom zijn prokaryoten ouder dan eukaryoten?
- Wat is de rol van calcereerklieren in de regenworm?
- Delen van een organisme die een belangrijke rol spelen bij het helpen van levende dingen die goed werken, worden opgeroepen?
- Hoe geslachtscellen de juiste genetische mix krijgen:een interdisciplinaire aanpak lost een eeuwenoude puzzel op
- Welke cellen produceren GEEN celwanden?
- Wat is de relatie tussen substraatconcentratie en enzymactiviteit?
- Welke 4 chemicaliën vormen DNA -strengen?
- Welke term beschrijft de theorie dat leven voortkomt uit leven?
- Wat is het oudste levende wezen op aarde?
- Symmetrische splitsing van disulfiden is snel en biocompatibel

- Onderzoekers brengen eiwitbeweging in kaart
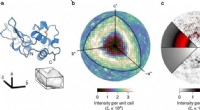
- Nieuw concept voor het identificeren van chemische combinaties met mogelijke gezondheidseffecten

- Nieuwe stof kan je helpen koel te blijven in de zomer, zelfs zonder airco

- Structuur van een bacteriële medicijnpomp onthult nieuwe manier om ziekenhuisinfecties tegen te gaan
 Hersendood hoe werkt
Hersendood hoe werkt  Nucleïnezuurgeheugen uitbreiden (NAM)
Nucleïnezuurgeheugen uitbreiden (NAM) Nieuwe studie laat zien hoe het Ebola-virus cellen infecteert
Nieuwe studie laat zien hoe het Ebola-virus cellen infecteert  Waar worden lipiden gesynthetiseerd in eukaryoten?
Waar worden lipiden gesynthetiseerd in eukaryoten?  Een voorbeeld van een relictgrens is de tussen?
Een voorbeeld van een relictgrens is de tussen?  Wat de dood van een eenzame inheemse man in Brazilië ons kan vertellen over onze wereldwijde toekomst
Wat de dood van een eenzame inheemse man in Brazilië ons kan vertellen over onze wereldwijde toekomst Thermo-elektriciteit:van warmte naar elektriciteit
Thermo-elektriciteit:van warmte naar elektriciteit Cilindrische nanodeeltjes dodelijker voor borstkanker
Cilindrische nanodeeltjes dodelijker voor borstkanker
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

