
Wetenschap
Is de moleculaire massa kaarsenwas minder dan 100?
Kaarswax is voornamelijk gemaakt van koolwaterstoffen, met name lange-chain alkanen. Deze alkanen hebben de algemene formule C n H 2n+2 .
Dit is de reden waarom de moleculaire massa kaarsenwas waarschijnlijk * groter * dan 100 is:
* lange ketens: De "N" in de formule vertegenwoordigt het aantal koolstofatomen in de keten. Candle Wax gebruikt meestal alkanen met ketens die 20-40 koolstofatomen bevatten.
* Atomische gewichten: Koolstof heeft een atoomgewicht van 12 en waterstof heeft een atoomgewicht van 1. Zelfs met een relatief korte keten van 20 koolstoffen zou de moleculaire massa zijn (20 * 12) + (42 * 1) =282.
Daarom is de moleculaire massa kaarsenwas aanzienlijk groter dan 100.
 Oude boeren transformeerden Amazon en lieten een blijvende erfenis achter in het regenwoud
Oude boeren transformeerden Amazon en lieten een blijvende erfenis achter in het regenwoud Stijgende temperaturen veranderen wanneer en hoeveel mensen naar buiten gaan op openbare gronden
Stijgende temperaturen veranderen wanneer en hoeveel mensen naar buiten gaan op openbare gronden de Tiete, De belangrijkste rivier van Sao Paulo, wordt gefilterd door damreservoirs
de Tiete, De belangrijkste rivier van Sao Paulo, wordt gefilterd door damreservoirs Hoe het verschil tussen een monarch en een onderkoning te onderscheiden Butterfly
Hoe het verschil tussen een monarch en een onderkoning te onderscheiden Butterfly Hoe weet ik wanneer mijn zebravinkvogel zwanger is?
Hoe weet ik wanneer mijn zebravinkvogel zwanger is?
Hoofdlijnen
- Facebook verandert de manier waarop het 'nepnieuws'-verhalen identificeert
- Waarom interesseert zoölogist u?
- Als ribosomen botsen:hoe bacteriën opruimen na moleculaire crashes
- Hoe wordt de beweging van moleculen door een membraan tegen hun concentratie ten koste van ATP-energie genoemd?
- G2-fase: wat gebeurt er in deze subfase van de celcyclus?
- Antibiotica beschermen appels tegen bacterievuur, maar vernietigen ze het inheemse microbioom?
- Zijn katten en dolfijnen eencellig organisme?
- In het Ecuadoraanse Amazonegebied vormen vlinders een graadmeter voor de klimaatverandering
- Begrijpen hoe bacteriën voedsel zoeken en ernaar toe bewegen
- AI- en NMR-spectroscopie bepalen in recordtijd de configuratie van atomen
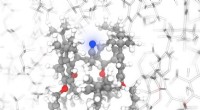
- Het pad van een metallodrug in een borstkankercel onthullen

- Veilige oplossing om olievlekken op te ruimen

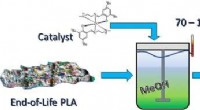
- Chemische recycling maakt nuttig product van bioplastic afval
- Elektrochemische zuurstofontwikkeling op Hf2B2Ir5-elektrodemateriaal

 Nieuw Russisch wapen kan 27 keer sneller dan geluid reizen
Nieuw Russisch wapen kan 27 keer sneller dan geluid reizen Wat is een lichte glazige rots gevormd van schuimige lava?
Wat is een lichte glazige rots gevormd van schuimige lava?  Waarom labelen alle kaarten de equator 0 breedtegraad en prime meridiaan lengtegraad?
Waarom labelen alle kaarten de equator 0 breedtegraad en prime meridiaan lengtegraad?  Genetica van waardplanten bepaalt welke micro-organismen ze aantrekken, zo blijkt uit onderzoek
Genetica van waardplanten bepaalt welke micro-organismen ze aantrekken, zo blijkt uit onderzoek  Een gestructureerde benadering van vroege alfabetisering levert uitstekende resultaten op voor kinderen in Nieuw-Zeeland
Een gestructureerde benadering van vroege alfabetisering levert uitstekende resultaten op voor kinderen in Nieuw-Zeeland  Brexit kan bijna 500 kosten, 000 banen in het VK:studeren
Brexit kan bijna 500 kosten, 000 banen in het VK:studeren Het lot van de Kalahari San
Het lot van de Kalahari San Hoe Stonehenge werkte
Hoe Stonehenge werkte
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

