
Wetenschap
Hoe verschillen de isotopen van het gegeven element van elkaar?
Hier is een uitsplitsing:
* Atomisch nummer: Alle isotopen van een bepaald element hebben hetzelfde atoomnummer, dat het aantal protonen in de kern vertegenwoordigt. Dit is wat het element zelf definieert.
* Massienummer: Isotopen verschillen in hun massatummer, het totale aantal protonen en neutronen in de kern.
* neutronen: Aangezien isotopen van hetzelfde element hetzelfde aantal protonen hebben, komt het verschil in hun massagummer van het verschillende aantal neutronen.
Voorbeeld:
* carbon-12 heeft 6 protonen en 6 neutronen (massaummer =12).
* carbon-14 heeft 6 protonen en 8 neutronen (massaummer =14).
Beide zijn koolstof omdat ze 6 protonen hebben, maar ze hebben verschillende aantallen neutronen, wat leidt tot verschillende massagummers.
Sleutelpunten:
* Isotopen hebben dezelfde chemische eigenschappen als gevolg van hetzelfde aantal elektronen.
* Isotopen kunnen stabiel of radioactief zijn, afhankelijk van de neutronen-protonverhouding.
* Sommige isotopen worden gebruikt in verschillende toepassingen, waaronder geneeskunde, datingtechnieken en kernenergie.
Hoofdlijnen
- Een ezelsverhaal:Nigeria wordt de belangrijkste exporthub voor verstoppingen
- Hoeveel bewijs is genoeg om een nieuwe mensensoort te verklaren?
- Hoe worden de bases op mRNA -strengen genoemd?
- Hoe vogelgenetica zich aanpast aan klimaatverandering
- Hoeveel DNA -moleculen zitten er in een chromosoom vlak voor mitiose?
- Welk organisme mist kernen in rode bloedcellen?
- De structuur van een eukaryote cel
- Zwarte wolven:de eerste genetisch gemodificeerde roofdieren?
- Waaruit bestaan weefsels in het lichaam?
- Een organisch materiaal voor de volgende generatie HVAC-technologieën

- Energieteam ontwikkelt processen om biogebaseerde vliegtuigbrandstof op te voeren

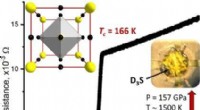
- Op weg naar conducteurs van de toekomst
- Een vereenvoudigde methode om olijfolie te categoriseren

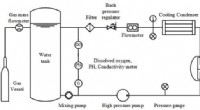
- Onderzoekers verkrijgen nieuwe resultaten over het corrosiegedrag van legeringsmaterialen onder extreme omgevingen
 Waarom zou wrijving de zwaartekracht beïnvloeden?
Waarom zou wrijving de zwaartekracht beïnvloeden?  Hoe 1 Gram te converteren naar Liter
Hoe 1 Gram te converteren naar Liter  Barry verzwakt, maar Amerikaanse functionarissen waarschuwen voor zware regenval, overstromingen, tornado's
Barry verzwakt, maar Amerikaanse functionarissen waarschuwen voor zware regenval, overstromingen, tornado's Een ongrijpbare ontbrekende schakel isoleren
Een ongrijpbare ontbrekende schakel isoleren Zijn dierentuinen onbedoeld medeplichtig aan de handel in wilde dieren? Het geval van een zeldzame Borneo-hagedis
Zijn dierentuinen onbedoeld medeplichtig aan de handel in wilde dieren? Het geval van een zeldzame Borneo-hagedis  Hoe lassen werkt
Hoe lassen werkt  Chemici ontdekken nieuwe reactiviteit van gespannen moleculen
Chemici ontdekken nieuwe reactiviteit van gespannen moleculen Voormalige Audi-baas sluit zich aan bij ex-VW-chef in dok over dieselgate
Voormalige Audi-baas sluit zich aan bij ex-VW-chef in dok over dieselgate
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


