
Wetenschap
Is de buitenste schaal van nikkel vol?
Dit is waarom:
* Nickel's Electron Configuration: Nikkel heeft een atoomnummer van 28, wat betekent dat het 28 elektronen heeft. De elektronenconfiguratie is [AR] 3D⁸ 4S².
* Elektronen verliezen om een ion te vormen: Om een stabiele configuratie te bereiken, verliest Nickel zijn twee 4S -elektronen en wordt hij Ni²⁺.
* Volledige buitenste schaal: Dit laat nikkel achter met de elektronenconfiguratie [AR] 3D⁸, die vergelijkbaar is met de stabiele configuratie van argon. De 3D -schaal kan maximaal 10 elektronen bevatten en nu heeft Nickel een volledige buitenste schaal.
Belangrijke opmerking: Dit geldt voor de * ionische * vorm van nikkel. In zijn * neutrale * toestand is de buitenste schaal van Nickel niet Vol, omdat het twee elektronen in de 4S -schaal heeft.
 Welke vier soorten organische moleculen worden in levende wezens aangetroffen?
Welke vier soorten organische moleculen worden in levende wezens aangetroffen?  Neurowetenschappers ontdekken nieuwe structuur van belangrijk eiwit in de hersenen
Neurowetenschappers ontdekken nieuwe structuur van belangrijk eiwit in de hersenen Hoe 36.000 begraven theezakjes de mondiale ontbinding helpen verklaren
Hoe 36.000 begraven theezakjes de mondiale ontbinding helpen verklaren  Waarom zouden Hirsch en Buchner Funnels niet worden gebruikt voor de filtratie van hete oplossingen?
Waarom zouden Hirsch en Buchner Funnels niet worden gebruikt voor de filtratie van hete oplossingen?  Proces verwijdert tegelijkertijd giftige metalen en zout om schoon water te produceren
Proces verwijdert tegelijkertijd giftige metalen en zout om schoon water te produceren
Hoofdlijnen
- Welk effect is de watercyclus op mensen?
- Wetenschappers ontdekken waarom rijp fruit gevoeliger is voor necrotrofe ziekteverwekkers dan onrijp fruit
- Hoe verschilt een longcel op het genetische niveau van hersencel?
- Wat is het gebruik van North Star of Polaris?
- Is hun geen limiet in hoe groot of klein een cel kan zijn?
- Hoe brengen planten microbiële vrienden en vijanden in evenwicht?
- Verschillende soorten brood Mold
- De verschillen tussen Catecholamines en Cortisol
- Orsini's adder:groei of voortplanting?
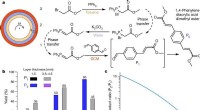
- Biodiesel maken met groene oplosmiddelen

- De kracht van zwavel ontsluiten in toekomstig medicijnontwerp

- Technieken voor het observeren van beton terwijl het hard wordt, kunnen de ontwikkeling van nieuw cement vergemakkelijken

- Studie gebruikt neutronen om licht te laten schijnen op het afsluiten van kankercellen

- Een nieuwe manier om opeenvolgingen van chemische reacties te automatiseren
 Welke eenvoudige machines zitten in een grasmaaier
Welke eenvoudige machines zitten in een grasmaaier  Wat voor soort Allele slaat een generatie over?
Wat voor soort Allele slaat een generatie over?  Studie identificeert belangrijke belemmeringen voor de financiering van een duurzame oceaaneconomie
Studie identificeert belangrijke belemmeringen voor de financiering van een duurzame oceaaneconomie Kleine trillende belletjes kunnen tot een betere waterbehandeling leiden
Kleine trillende belletjes kunnen tot een betere waterbehandeling leiden  Waarom zijn gloeilampen gevuld met argon en niet met lucht?
Waarom zijn gloeilampen gevuld met argon en niet met lucht?  Het benutten van symmetrieën:de computationele studie van solide oplossingen versnellen
Het benutten van symmetrieën:de computationele studie van solide oplossingen versnellen Is nikkel een betere katalysator dan koper in een autothermische hervorming?
Is nikkel een betere katalysator dan koper in een autothermische hervorming?  NASA's Juno-missie detecteert Jupiter-golftreinen
NASA's Juno-missie detecteert Jupiter-golftreinen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

