
Wetenschap
Waarom verschillen de eigenschappen van natriumchloride van metaal- en chloorgas?
Hier is een uitsplitsing:
Natrium (NA):
* metaal: Zacht, zilverachtig wit, zeer reactief, geleidt elektriciteit en warmte goed.
* reageert krachtig met water: Geeft waterstofgas vrij en vormt een sterk alkalische oplossing.
chloor (CL):
* gas: Geelgroen, scherp, giftig, zeer reactief.
* Sterke oxidator: Kan reageren met veel stoffen, wat leidt tot vuur of explosies.
Natriumchloride (NaCl):
* solide: Wit kristallijn, bros, niet-toxisch, leidt geen elektriciteit in vaste vorm, lost gemakkelijk op in water.
Waarom het verschil?
* ionische binding: Natrium en chloor reageren gewelddadig, waarbij natrium een elektron op chloor opgeeft. Dit creëert positief geladen natriumionen (Na+) en negatief geladen chloride-ionen (Cl-).
* Sterke elektrostatische aantrekkingskracht: De tegengesteld geladen ionen worden tot elkaar aangetrokken en vormen een kristalroosterstructuur. Deze sterke elektrostatische kracht is wat natriumchloride zijn unieke eigenschappen geeft.
Hier is hoe de eigenschappen verschillen:
* Reactiviteit: Natriumchloride is veel minder reactief dan natrium of chloor. De ionische binding stabiliseert de ionen, waardoor ze minder geneigd zijn om deel te nemen aan verdere reacties.
* Staat van materie: De sterke ionische bindingen in natriumchloride creëren een vaste stof bij kamertemperatuur. Dit is in tegenstelling tot het metalen natrium, dat vast is, en chloor, dat een gas is.
* geleidbaarheid: Natriumchloride leidt elektriciteit wanneer opgelost in water omdat de ionen vrij zijn om te bewegen. In zijn vaste vorm zijn de ionen echter op vergrendeld in het kristalrooster en kunnen ze niet vrij bewegen. Dit verschilt van metallisch natrium, dat elektriciteit in vaste vorm leidt.
* toxiciteit: Chloorgas is giftig, terwijl natriumchloride niet giftig is. De ionische binding verandert de reactiviteit en toxiciteit van de samenstellende elementen aanzienlijk.
In wezen verandert de vorming van ionische bindingen de chemische en fysische eigenschappen van natrium en chloor drastisch, wat resulteert in een volledig andere stof met eigen unieke kenmerken.
 Wat gebruik je om een munt van zilver schoon te maken?
Wat gebruik je om een munt van zilver schoon te maken?  Wat gebeurt er als de moleculen in een vloeistof bewegen?
Wat gebeurt er als de moleculen in een vloeistof bewegen?  Glycanen zijn cruciaal bij COVID-19-infectie
Glycanen zijn cruciaal bij COVID-19-infectie Wat gebeurt er met een kooktemperatuur als de druk afneemt?
Wat gebeurt er met een kooktemperatuur als de druk afneemt?  Ingenieurs verhogen de efficiëntie bij het omzetten van broeikasgassen in ethyleen
Ingenieurs verhogen de efficiëntie bij het omzetten van broeikasgassen in ethyleen
Hoofdlijnen
- Rolmodelstamcellen:hoe immuuncellen zichzelf kunnen vernieuwen
- Wetenschappers ontdekken methode om voedselverspilling om te zetten in biobrandstoffen
- Wat doet een spirillius?
- Hoe heet de stof rond dooier?
- Waartoe leidt hypothese?
- Het leefgebied van de panda krimpt, steeds meer gefragmenteerd worden
- Wat is de site van primaire sensorische integratie in de hersenen die worden genoemd?
- Welke invloed heeft de zuurschok in het voorjaar op waterorganismen?
- Experimenten tonen aan dat de gegevens over het vroege leven volledig 'vals-positieven' kunnen zijn
- Ontwerpen en herbestemmen van celreceptoren

- Gecontroleerde afgifte van kunstmest met behulp van biopolymeerchips

- Recycling van polypropyleen uit tapijtafval

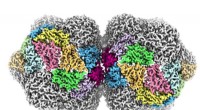
- Verwoestend plantenvirus wordt in atomaire details onthuld
- Machine learning kan ons leren hoe we de productie van materialen schoner en duurzamer kunnen maken
 Ze kwamen met een nieuwe reeks doelen om de natuurlijke wereld te beschermen. Hier is hoe
Ze kwamen met een nieuwe reeks doelen om de natuurlijke wereld te beschermen. Hier is hoe Dynamische stalling bij hoge snelheden begrijpen
Dynamische stalling bij hoge snelheden begrijpen Proces van het synthetiseren van een RNA -streng uit een DNA -sjabloonstreng?
Proces van het synthetiseren van een RNA -streng uit een DNA -sjabloonstreng?  Geschatte kwantumklonen:de nieuwe manier van afluisteren in kwantumcryptografie
Geschatte kwantumklonen:de nieuwe manier van afluisteren in kwantumcryptografie De evolutie van intelligentie en waarom onze hersenen zijn gekrompen
De evolutie van intelligentie en waarom onze hersenen zijn gekrompen  Reageert beryllium met zuurstof?
Reageert beryllium met zuurstof?  Hoe breekt kalksteen?
Hoe breekt kalksteen?  Grafieken met een Ti 84-calculator
Grafieken met een Ti 84-calculator
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

