
Wetenschap
Wat is de balansvergelijking voor volledige verbranding van C18H36?
De uitgebalanceerde vergelijking voor de volledige verbranding van \(C_{18}H_{36}\) is:
$$2C_{18}H_{36} + 49O_2 \pijl naar rechts 36CO_2 + 36H_2O$$
In deze vergelijking reageren twee moleculen \(C_{18}H_{36}\) met 49 moleculen zuurstof (\(O_2\)) om 36 moleculen koolstofdioxide (\(CO_2\)) en 36 moleculen koolstofdioxide te produceren water(\(H_2O\)). Deze reactie vertegenwoordigt de volledige verbranding van \(C_{18}H_{36}\), wat betekent dat alle koolstofatomen in de brandstof worden omgezet in koolstofdioxide en alle waterstofatomen worden omgezet in water.
 Dieetvetten werken samen met druiventannines om de wijnsmaak te beïnvloeden
Dieetvetten werken samen met druiventannines om de wijnsmaak te beïnvloeden Wat is de chemische formule voor epoxyhars?
Wat is de chemische formule voor epoxyhars?  Defect- en interface-engineering voor e-NRR onder omgevingsomstandigheden
Defect- en interface-engineering voor e-NRR onder omgevingsomstandigheden Wetenschappers testen met succes nieuwe, veiligere titaniumplaat voor herstel van botweefsel
Wetenschappers testen met succes nieuwe, veiligere titaniumplaat voor herstel van botweefsel De chemie van de aarde modelleren:het onzichtbare zichtbaar maken
De chemie van de aarde modelleren:het onzichtbare zichtbaar maken
 NASA-NOAA satellietvolgsysteem Super Typhoon Mangkhut
NASA-NOAA satellietvolgsysteem Super Typhoon Mangkhut Biologische oceanograaf ontleedt de verbanden tussen menselijke invloeden op de oceaan en hun effecten op menselijke systemen
Biologische oceanograaf ontleedt de verbanden tussen menselijke invloeden op de oceaan en hun effecten op menselijke systemen Ultragevoelige metingen houden nucleaire explosies in de gaten
Ultragevoelige metingen houden nucleaire explosies in de gaten Technologie voor kleine boerderijen vermindert ontbossing, klimaatverandering
Technologie voor kleine boerderijen vermindert ontbossing, klimaatverandering Abiotische en biotische factoren van poolstreken
Abiotische en biotische factoren van poolstreken
Hoofdlijnen
- Onderzoekers ontdekken nieuwe overspraak tussen fytohormonen ethyleen en auxine
- 10 misvattingen over de griep
- Endoplasmatisch reticulum (ruw en glad): structuur en functie (met diagram)
- Waar bevinden zich de mitochondriën in de dierlijke cel?
- Over leverfuncties in het menselijk lichaam
- Fossil bevat nieuwe inzichten in hoe vissen op het land zijn geëvolueerd
- Hoe vaak komt agressie bij Britse honden voor?
- Hoe sociale dynamiek de darmmicroben van wilde maki's beïnvloedt
- Onderzoek toont aan dat het verwijderen van invasieve planten de biodiversiteit in beekwateren kan vergroten
- Studie onthult nieuwe bevindingen over synergie van antimicrobiële geneesmiddelen
- Selectief kooldioxide omzetten in methaan of ethaan

- Doorbraak in lignine-onderzoek - bolvormige deeltjes vermenigvuldigen de enzymefficiëntie

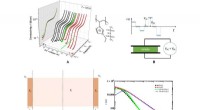
- Capaciteit van dunne films die gepolymeriseerde ionische vloeistoffen bevatten
- Zelfreinigend beton kan gebouwen er als nieuw uit laten zien

 Wat is de sfeer van Het tij stijgt en valt?
Wat is de sfeer van Het tij stijgt en valt?  Componenten van lysebuffers
Componenten van lysebuffers  5 landbouwtechnologieën die de wereld hebben veranderd
5 landbouwtechnologieën die de wereld hebben veranderd  Een nieuwe strategie voor het fabriceren van pn-overgangen in enkelkristallijne Si-nanodraden, draaien
Een nieuwe strategie voor het fabriceren van pn-overgangen in enkelkristallijne Si-nanodraden, draaien Hoe zelfs een oppervlakkige aanraking met de wet het leven van een jonge man permanent kan bederven - vooral als hij zwart is?
Hoe zelfs een oppervlakkige aanraking met de wet het leven van een jonge man permanent kan bederven - vooral als hij zwart is? Kun je een baby krijgen op Mars?
Kun je een baby krijgen op Mars?  Wetenschappers ontdekken dat darmbacteriën in bijen antibioticaresistente genen naar elkaar verspreiden
Wetenschappers ontdekken dat darmbacteriën in bijen antibioticaresistente genen naar elkaar verspreiden Boerenmarktverkopers hebben training nodig om voedselveiligheidspraktijken te verbeteren
Boerenmarktverkopers hebben training nodig om voedselveiligheidspraktijken te verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

