
Wetenschap
Hcl nahco3 nacl H2O CO2 reactie-enthalpie?
HCl + NaHCO3 + NaCl + H2O + CO2
De enthalpieverandering voor deze reactie kan worden berekend met behulp van de volgende vergelijking:
ΔH =ΣnΔHf(producten) - ΣnΔHf(reactanten)
waarbij ΔH de enthalpieverandering is, n het aantal mol van elke stof is, en ΔHf de standaardvormingsenthalpie van elke stof is.
De standaard vormingsenthalpieën voor de stoffen die bij de reactie betrokken zijn, zijn:
HCI:-167,2 kJ/mol
NaHC03:-950,8 kJ/mol
NaCl:-411,2 kJ/mol
H2O:-285,8 kJ/mol
CO2:-393,5 kJ/mol
Als we deze waarden in de vergelijking invullen, krijgen we:
ΔH =[1(-393,5 kJ/mol) + 1(-411,2 kJ/mol)] - [1(-167,2 kJ/mol) + 1(-950,8 kJ/mol)]
ΔH =-804,7 kJ/mol + 1118 kJ/mol
ΔH =313,3 kJ/mol
Daarom is de enthalpieverandering voor de reactie 313,3 kJ/mol. Dit betekent dat de reactie endotherm is, wat betekent dat deze warmte uit de omgeving absorbeert.
 Hoe hebben Tsunami's invloed op mensenlevens?
Hoe hebben Tsunami's invloed op mensenlevens?  Afhaalmaaltijden - de milieukosten van het verpakken van onze favoriete fastfood
Afhaalmaaltijden - de milieukosten van het verpakken van onze favoriete fastfood Verwachte toename van neerslag is slecht nieuws voor de waterkwaliteit
Verwachte toename van neerslag is slecht nieuws voor de waterkwaliteit Inzicht in hoe vogels reageren op extreem weer kan bijdragen aan natuurbehoudsinspanningen
Inzicht in hoe vogels reageren op extreem weer kan bijdragen aan natuurbehoudsinspanningen  Overstromingen door orkaan Harvey veroorzaken tal van zorgen voor de volksgezondheid
Overstromingen door orkaan Harvey veroorzaken tal van zorgen voor de volksgezondheid
Hoofdlijnen
- In welk jaar bouwde Francis Crick het DNA-model?
- Wat zijn de voor- en nadelen van flowcytometrie?
- Op de loer in genomische schaduwen:hoe gigantische virussen de evolutie van algen voeden
- Hoe consumenten de voordelen van genetisch gemodificeerd voedsel kunnen laten zien
- Is er echt een kurkcrisis?
- Onderzoekers genereren tomaten met verbeterde antioxiderende eigenschappen door genetische manipulatie
- Wat beschrijft het beste hoe chromosomen tijdens mitose naar de polen van de spil bewegen?
- Wat doet een isomerase-enzym?
- AI-aangedreven virtuele rat biedt inzicht in hoe hersenen complexe, gecoördineerde bewegingen controleren
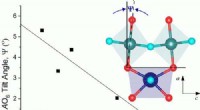
- Kennis opbouwen van veranderingen in de uraniumchemie
- Zeeslakverbinding vermindert het risico op kanker

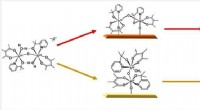
- Een nieuwe katalysator voor watersplitsing die het beste van twee werelden is
- Team ontwikkelt ontbrekende schakel naar circulaire economie en pakt wereldwijde verspilling aan
- Voor een echte oorlog tegen afval, de mode-industrie moet meer uitgeven aan onderzoek

 Simulaties lokaliseren defecten op atomair niveau in nanostructuren van zonnecellen
Simulaties lokaliseren defecten op atomair niveau in nanostructuren van zonnecellen Wat zijn de voordelen van het zijn van marien bioloog?
Wat zijn de voordelen van het zijn van marien bioloog?  Wetenschappers onderzoeken transport van nanodeeltjes in het menselijk lichaam
Wetenschappers onderzoeken transport van nanodeeltjes in het menselijk lichaam Bepaling van de hoeveelheid negatieve luchtmachines per kubieke voet
Bepaling van de hoeveelheid negatieve luchtmachines per kubieke voet Analyse van instellingen die minderheden bedienen, laat gelaagde processen zien om de capaciteiten van studenten op te bouwen
Analyse van instellingen die minderheden bedienen, laat gelaagde processen zien om de capaciteiten van studenten op te bouwen  Wat is de eenheid voor elektrisch veld?
Wat is de eenheid voor elektrisch veld?  Quibi:de nieuwe mobielgerichte short-form streamingdienst
Quibi:de nieuwe mobielgerichte short-form streamingdienst Satellieten analyseren het ontwikkelende golfpotentieel Tropische cycloon twee
Satellieten analyseren het ontwikkelende golfpotentieel Tropische cycloon twee
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

