
Wetenschap
Wat zijn de toepassingen van jodiumtrichloride?
- Katalysator:Jodiumtrichloride wordt veel gebruikt als Lewis-zuurkatalysator bij organische synthese. Het vergemakkelijkt een verscheidenheid aan reacties, waaronder additie-, substitutie-, cyclisatie- en oxidatiereacties. Het wordt bijvoorbeeld gebruikt in de Friedel-Crafts-acyleringsreactie, waar het de reactie tussen een aromatische verbinding en een zuurchloride bevordert.
- Oxidatiemiddel:Jodiumtrichloride werkt als een sterk oxidatiemiddel vanwege de aanwezigheid van zeer reactieve chlooratomen. Het is in staat een breed scala aan anorganische en organische substraten te oxideren. In het laboratorium kan het bijvoorbeeld worden gebruikt om ijzerzouten te oxideren tot ijzerzouten.
- Analytische chemie:Jodiumtrichloride vindt toepassing in kwalitatieve en kwantitatieve analyse. Het wordt gebruikt als selectief reagens voor de detectie en bepaling van verschillende ionen, zoals sulfiden, thiosulfaten en arsenieten.
- Desinfectie:Jodiumtrichloride vertoont sterke bacteriedodende en virusdodende eigenschappen, waardoor het nuttig is als desinfecterend en antiseptisch middel. Het wordt vaak gebruikt in waterzuiveringssystemen, zwembaden en ziekenhuizen om schadelijke micro-organismen te elimineren.
- Synthetische toepassingen:Jodiumtrichloride is betrokken bij de synthese van verschillende organische en anorganische verbindingen. Het wordt bijvoorbeeld gebruikt bij de productie van jodiummonochloride, jodiumpentafluoride en bepaalde organojodiumverbindingen.
- Etsen en graveren:Jodiumtrichloride wordt in de metaalverwerkende industrie gebruikt voor ets- en graveerprocessen. Het is bijzonder effectief bij het etsen van metalen zoals koper en staal.
Vanwege de hoge reactiviteit moet jodiumtrichloride zorgvuldig worden gehanteerd en moet het met passende veiligheidsmaatregelen worden gebruikt om potentiële gevaren te voorkomen.
 Chemici leren een enzym een nieuwe truc, met potentieel voor het bouwen van nieuwe moleculen
Chemici leren een enzym een nieuwe truc, met potentieel voor het bouwen van nieuwe moleculen Naam en formule voor de chemische stof die altijd ontstaat bij een neutralisatiereactie?
Naam en formule voor de chemische stof die altijd ontstaat bij een neutralisatiereactie?  Wat doen mensen om zure regen erger te maken?
Wat doen mensen om zure regen erger te maken?  Bestaat Bonding in stoffen die bestaan uit discrete moleculen?
Bestaat Bonding in stoffen die bestaan uit discrete moleculen?  Hebben alle delen van een homogeen mengsel dezelfde samenstelling?
Hebben alle delen van een homogeen mengsel dezelfde samenstelling?
 Waar vindt fotosynthese plaats?
Waar vindt fotosynthese plaats?  Vroege klimaatterugbetaling met hogere emissiereducties
Vroege klimaatterugbetaling met hogere emissiereducties Van rook die de wereld rondgaat tot aerosolniveaus, NASA observeert bosbranden in Australië
Van rook die de wereld rondgaat tot aerosolniveaus, NASA observeert bosbranden in Australië Dodelijke vijanden in bondgenoten veranderen? Mieren kunnen dat
Dodelijke vijanden in bondgenoten veranderen? Mieren kunnen dat  Wetenschappers bieden routekaart voor onderzoek naar verband tussen klimaat en gewapend conflict
Wetenschappers bieden routekaart voor onderzoek naar verband tussen klimaat en gewapend conflict
Hoofdlijnen
- Hoe lepra werkt
- Zijn genderverschillen vooraf bepaald?
- Waar vindt de opname van aminozuren en enkelvoudige suikers plaats?
- Waarom één op de ogen gericht virus een nuttig hulpmiddel voor de overdracht van genen zou kunnen zijn
- Een universele voedsel- en alarmsignaal gevonden in zoogdierbloed
- Chinese fruitvlieggenomen onthullen mondiale migraties en herhaalde evolutie
- Hoe helpt DNA de homeostase in stand te houden?
- Hoe binnendringende ziekteverwekkers de afweer van plantencellen uitschakelen
- Een 'aardbeving' in de cel:wetenschappers ontdekken hoe een wijziging van de nucleaire lamina zijn vorm behoudt
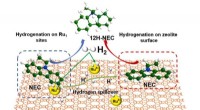
- Synergistische katalysatoren voor zeer efficiënte waterstofopslag
- De nieuw ontdekte architectuur van een koper-nitrenoïde-complex kan een revolutie teweegbrengen in de chemische synthese

- Hoe licht kan een opvouwbare en duurzame batterij zijn?

- Chemicus maakt de volgende generatie neurowetenschappelijke tools

- Coördinatiepolymeerglas biedt solide ondersteuning voor waterstofbrandstofcellen

 De keten doorbreken - een groene toekomst voor de chemie katalyseren
De keten doorbreken - een groene toekomst voor de chemie katalyseren Verbetering van de weersvoorspelling met een nieuwe IASI-kanaalselectiemethode
Verbetering van de weersvoorspelling met een nieuwe IASI-kanaalselectiemethode Moeten we bedreigde diersoorten kweken?
Moeten we bedreigde diersoorten kweken?  Oudste melkwegprotocluster vormt koninginnenhof
Oudste melkwegprotocluster vormt koninginnenhof Woont er iemand in de buurt van de vulkaan Eyjafjallajokull?
Woont er iemand in de buurt van de vulkaan Eyjafjallajokull?  Wetenschappers onderzoeken hoe cerium in het universum wordt geproduceerd
Wetenschappers onderzoeken hoe cerium in het universum wordt geproduceerd  Het meten van de gevolgen voor de volksgezondheid na rampen
Het meten van de gevolgen voor de volksgezondheid na rampen Hoe plannen om op Mars te leven onze huizen op aarde kunnen hervormen
Hoe plannen om op Mars te leven onze huizen op aarde kunnen hervormen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

