
Wetenschap
Wat gebeurt er als natrium in water wordt gedruppeld?
Wanneer natriummetaal aan water wordt toegevoegd, reageert het snel met de watermoleculen, waarbij elektronen worden overgedragen van natriumatomen naar zuurstofatomen in de watermoleculen. Deze overdracht van elektronen zorgt ervoor dat de natriumatomen positief geladen ionen (Na+) worden, terwijl de zuurstofatomen een negatieve lading krijgen en hydroxide-ionen (OH-) vormen.
De chemische vergelijking voor deze reactie is:
2Na(s) + 2H2O(l) → 2NaOH(aq) + H2(g)
De reactie tussen natrium en water is ongelooflijk krachtig en produceert een grote hoeveelheid warmte en waterstofgas. De tijdens de reactie gegenereerde warmte kan ervoor zorgen dat het water gaat koken en spatten, terwijl het geproduceerde waterstofgas brandbaar is en spontaan kan ontbranden in de lucht.
Het is essentieel op te merken dat deze reactie met uiterste voorzichtigheid en passende veiligheidsmaatregelen moet worden uitgevoerd, aangezien deze potentieel gevaarlijk kan zijn vanwege het risico op brand en de bijtende eigenschappen van natriumhydroxide.
 Nuttige microben inhaleren koolstofdioxide via een poreuze cilindrische elektrode en scheiden nuttige chemicaliën uit
Nuttige microben inhaleren koolstofdioxide via een poreuze cilindrische elektrode en scheiden nuttige chemicaliën uit Wat zijn vijf polymeren in een huis?
Wat zijn vijf polymeren in een huis?  De voetafdruk verkleinen van een broeikasgas dat krachtiger is dan koolstofdioxide
De voetafdruk verkleinen van een broeikasgas dat krachtiger is dan koolstofdioxide Welke groepen ondergaan hydrolyse?
Welke groepen ondergaan hydrolyse?  Hoe het vriespunt van water te verhogen
Hoe het vriespunt van water te verhogen
Hoofdlijnen
- Hoe octopussen, inktvissen en inktvissen het ‘centrale dogma’ van de genetica trotseren
- Onderzoekers ontdekken hoe weefsels en organen tijdens de embryogenese worden vormgegeven
- Hoe superbacteriën spiegelbeelden gebruiken om antibioticaresistentie te creëren
- Hoe zijn meer stuifmeelkorrels belangrijk in termen van reproductief succes?
- Ja,
- Wetenschappers vinden ontbrekende aanwijzing voor de manier waarop HIV-hackcellen zichzelf voortplanten
- Wat is de functie van lymfeklieren?
- Nucleïnezuren: structuur, functie, typen en voorbeelden
- In populaties van microben, bio-ingenieurs vinden een balans tussen tegengestelde genomische krachten
- Een manier om de absolute stereochemie van kleine, organische moleculen
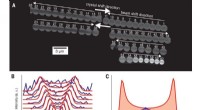
- Sinaasappelschilolie opzuigen tot nieuwe, aangename aromastoffen

- Forensische onderzoekers vinden een nauwkeurigere manier om de leeftijd van overledenen te schatten

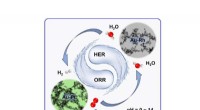
- Chemici ontwikkelen edelmetaal-aerogels voor elektrochemische waterstofproductie
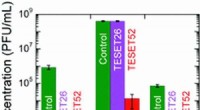
- Zelfsteriliserend polymeer blijkt effectief tegen medicijnresistente pathogenen
 Hoe zal de WK-bal van 2014 uitwijken?
Hoe zal de WK-bal van 2014 uitwijken?  Waarom zijn mannelijke muizen bang voor bananen?
Waarom zijn mannelijke muizen bang voor bananen?  Robotvissen helpen begrijpen hoe dieren bewegen
Robotvissen helpen begrijpen hoe dieren bewegen  DR Congo-regering geeft groen licht voor herstart kernreactor
DR Congo-regering geeft groen licht voor herstart kernreactor Kernmonsters van havensediment bieden historisch bewijs van oud Romeins sanitair
Kernmonsters van havensediment bieden historisch bewijs van oud Romeins sanitair Patronen blootleggen in brandende bosbranden in Californië
Patronen blootleggen in brandende bosbranden in Californië Duitse regering, industrie terug Ruimtehavenplan Noordzee
Duitse regering, industrie terug Ruimtehavenplan Noordzee Waarom het gezicht van de westerse oorlog ons een verkeerd beeld geeft van conflicten?
Waarom het gezicht van de westerse oorlog ons een verkeerd beeld geeft van conflicten?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

