
Wetenschap
Wat is de atomaire structuur van ijzer?
Atoomnummer: 26
Protonen: In de kern van een ijzeratoom bevinden zich 26 protonen. Het aantal protonen in de kern definieert het atoomnummer en bepaalt de identiteit van het element.
Neutronen: IJzeratomen hebben gewoonlijk 30 neutronen in de kern, maar andere isotopen van ijzer kunnen een variërend aantal neutronen hebben. Neutronen dragen bij aan de totale massa van het atoom, maar dragen geen elektrische lading.
Elektronen: IJzer heeft 26 elektronen die in specifieke energieniveaus of schillen rond de kern cirkelen. Deze elektronen zijn gerangschikt in schillen op basis van hun energieniveau.
De elektronenconfiguratie van ijzer is:
- K-schil:2 elektronen
- L-schil:8 elektronen
- M-schil:14 elektronen
- N-schil:2 elektronen
Valentie-elektronen: De buitenste schil van een atoom, bekend als de valentieschil, speelt een cruciale rol bij chemische binding. In ijzer is de valentieschil de N-schil, die 2 elektronen heeft. Deze valentie-elektronen zijn verantwoordelijk voor deelname aan chemische reacties en het vormen van bindingen met andere atomen.
De elektronische configuratie van ijzer kan worden weergegeven als [Ar]3d64s2, wat de aanwezigheid van zes elektronen in de 3D-subshell en twee elektronen in de 4s-subshell aangeeft.
Atoomorbitalen: De elektronen in de verschillende schillen bezetten atomaire orbitalen, dit zijn gebieden rond de kern waar waarschijnlijk elektronen worden aangetroffen. De 3D-orbitalen spelen een belangrijke rol bij het bepalen van de magnetische eigenschappen en het chemische gedrag van ijzer.
De atomaire structuur van ijzer is verantwoordelijk voor de verschillende eigenschappen ervan, waaronder de sterkte, duurzaamheid, magnetische gevoeligheid en het vermogen om legeringen met andere metalen te vormen. IJzer is een essentieel element in veel industrieën en is door de geschiedenis heen van cruciaal belang geweest bij het vormgeven van de technologische vooruitgang van de menselijke beschaving.
 Wat gebeurt er als een atoom een ion vormt?
Wat gebeurt er als een atoom een ion vormt?  Is calciumcarbonaat oplosbaar in azijn?
Is calciumcarbonaat oplosbaar in azijn?  The next big thing:hoe brengen wetenschappers waterstofbrandstofcellen van het laboratorium naar het openbare leven?
The next big thing:hoe brengen wetenschappers waterstofbrandstofcellen van het laboratorium naar het openbare leven? Waarom poppen ballonnen wanneer ze in een hete auto worden achtergelaten?
Waarom poppen ballonnen wanneer ze in een hete auto worden achtergelaten?  Toekomstige biosensor voor continue monitoring met behulp van moleculaire lookalikes
Toekomstige biosensor voor continue monitoring met behulp van moleculaire lookalikes
 Langere levensduur niet afhankelijk van verhoogd energieverbruik
Langere levensduur niet afhankelijk van verhoogd energieverbruik Video:Visualisatie van de wereldwijde dooi
Video:Visualisatie van de wereldwijde dooi Inheemse indringers – een kier in het pantser van het ecologisch beleid?
Inheemse indringers – een kier in het pantser van het ecologisch beleid?  Diverse geografie van de 82 grootste eilanden van Groot-Brittannië onthuld
Diverse geografie van de 82 grootste eilanden van Groot-Brittannië onthuld Natuurlijke landschappen? Wetenschappers roepen op tot een paradigmaverschuiving in restauratieprojecten
Natuurlijke landschappen? Wetenschappers roepen op tot een paradigmaverschuiving in restauratieprojecten
Hoofdlijnen
- Waar wordt koolstofdioxide gevormd tijdens het glucosemetabolisme?
- Achterbakse bacteriën:een nieuwe behandeling voor infectie?
- Wat is de functie van substage in de microscoop?
- Onderzoekers onthullen het mechanisme waarmee cellulaire kernen hun positie in spiercellen bereiken
- Wetenschappers ontwikkelen nieuwe aanpak om belangrijke onontdekte functies van eiwitten te identificeren
- Wat zegt Polly? Uit gemeenschapswetenschappelijke gegevens blijkt dat er verschillen tussen soorten bestaan in het vocale leren van papegaaien
- Hoe kan het begrijpen van verkeerd gevouwen eiwitten de behandeling van ziekten helpen verbeteren?
- Hoe sociale dynamiek de darmmicroben van wilde maki's beïnvloedt
- Studie:Hoe een unieke familie bacteriën zich verbergt voor het immuunsysteem
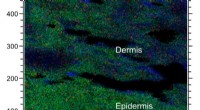
- Nieuwe methode brengt chemicaliën in de huid in kaart
- Wetenschappers ontdekken werkingsmechanisme voor veelbelovende kankerverbinding

- Onderzoek levert nieuw ontwerpprincipe op voor watersplitsende katalysatoren

- Een keramische aerogel gemaakt met nanokristallen en ingebed in een matrix voor gebruik in thermische isolatietoepassingen

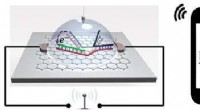
- Biosensor-chip detecteert draadloos single-nucleotide polymorfisme, met hogere gevoeligheid
 Punjab tekstboekbord Lahore scheikunde van 10 uur les?
Punjab tekstboekbord Lahore scheikunde van 10 uur les?  Feiten over éénmotorige vliegtuigen
Feiten over éénmotorige vliegtuigen  Amazon dringt er bij de politie op aan om gezichtsherkenningstool niet te verkopen
Amazon dringt er bij de politie op aan om gezichtsherkenningstool niet te verkopen Wetenschappers leggen uit waarom meridionaal warmtetransport wordt onderschat
Wetenschappers leggen uit waarom meridionaal warmtetransport wordt onderschat  Hoe krijg je een vierkantswortelantwoord van een vierkantswortel op een TI-84
Hoe krijg je een vierkantswortelantwoord van een vierkantswortel op een TI-84 Hoe delen van een plant met elkaar kunnen 'praten' ten bate van het geheel
Hoe delen van een plant met elkaar kunnen 'praten' ten bate van het geheel  Rifvissen erven tolerantie voor opwarmende oceanen
Rifvissen erven tolerantie voor opwarmende oceanen Hoe een spin te identificeren door Web Pattern
Hoe een spin te identificeren door Web Pattern
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

