
Wetenschap
Hoeveel lithiumatomen zitten er in 12,0 g?
Het antwoord:4,14 x 10^23
Uitleg:
Om het aantal atomen in 12,0 g lithium te berekenen, kunnen we de volgende formule gebruiken:
Aantal atomen =(massa van de stof in gram) / (atoommassa van de stof in gram per mol) x (getal van Avogadro)
De atoommassa van lithium is 6,941 g/mol en het getal van Avogadro is 6,022 x 10^23 atomen/mol.
Als we de gegeven waarden in de formule vervangen, krijgen we:
Aantal atomen =(12,0 g) / (6,941 g/mol) x (6,022 x 10^23 atomen/mol)
Aantal atomen ≈ 4,14 x 10^23 atomen
Daarom zijn er ongeveer 4,14 x 10^23 lithiumatomen in 12,0 g lithium.
 Onderzoek toont aan waarom het gewone explosieve PETN soms faalt
Onderzoek toont aan waarom het gewone explosieve PETN soms faalt  Wordt hetzelfde gas geproduceerd bij verschillende chemische reacties?
Wordt hetzelfde gas geproduceerd bij verschillende chemische reacties?  Een kosteneffectieve methode om chemische bouwstenen te synthetiseren
Een kosteneffectieve methode om chemische bouwstenen te synthetiseren De overeenkomsten tussen een schilderij van Van Gogh en een golfbal
De overeenkomsten tussen een schilderij van Van Gogh en een golfbal Draagbare sensoren kunnen biotechnologie gebruiken om persoonlijke, milieugegevens
Draagbare sensoren kunnen biotechnologie gebruiken om persoonlijke, milieugegevens
 Japan lanceert onderzoek naar vermoedelijke Chinese koraalstroperij
Japan lanceert onderzoek naar vermoedelijke Chinese koraalstroperij NASA observeert extreme regenval boven Zuid-Californië
NASA observeert extreme regenval boven Zuid-Californië Hoe onze planten dieven zijn geworden om te overleven
Hoe onze planten dieven zijn geworden om te overleven  4,6-magnitude aardbeving rammelt Hawaiis Big Island
4,6-magnitude aardbeving rammelt Hawaiis Big Island In het opwarmende Noordpoolgebied, grote rivieren vertonen verrassende veranderingen in koolstofchemie
In het opwarmende Noordpoolgebied, grote rivieren vertonen verrassende veranderingen in koolstofchemie
Hoofdlijnen
- Onderzoekers onthullen een verborgen eigenschap in de genomen van Mycobacterium die de aanpassing aan stress regelt
- Geen microben? probleem voor rupsen
- Hoe hoog kan een boom worden?
- Het verhaal van evolutie geschreven in fosfor
- Vijf soorten isolatie in de biologie
- Veertien jaar na de olieramp in de Golf van Mexico gaan de endemische vissen een onzekere toekomst tegemoet
- Twee populaties die gescheiden zijn door een bergketen kunnen zich niet langer kruisen om vruchtbare nakomelingen te produceren. Dit is een voorbeeld van?
- In de stad levende pimpelmezen kunnen grotere eieren leggen vanwege wat ze eten
- Zijn linkshandigen beter in sport?
- Belangrijkste mechanismen van luchtwegontspanning bij astma onthuld in nieuwe studie
- Eenvoudige methode om hoogwaardige bioactieve stoffen te extraheren uit eencellige algenolie
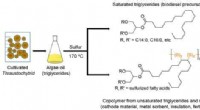
- Schoner maken, groenere kunststoffen uit afvalvisdelen

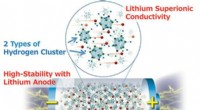
- Nieuw onderzoek toont aan dat alle solid-state batterijen met de hoogste energiedichtheid nu mogelijk zijn
- Synthese bij hoge temperatuur onder druk helpt eigenschappen van metalen en keramiek te combineren

 Een microscoop in een microscoop
Een microscoop in een microscoop Hoe een enorm schip te recyclen – veilig en duurzaam
Hoe een enorm schip te recyclen – veilig en duurzaam Een nieuwe kijk op de chemie van de binnenlucht
Een nieuwe kijk op de chemie van de binnenlucht De haalbaarheid van transformatietrajecten voor het behalen van het Klimaatakkoord van Parijs
De haalbaarheid van transformatietrajecten voor het behalen van het Klimaatakkoord van Parijs Wat beperkt het vermogen van planten om water uit droge grond te halen?
Wat beperkt het vermogen van planten om water uit droge grond te halen?  Opinie:Nobelprijswinnende economie van klimaatverandering is misleidend en gevaarlijk, en hier is waarom
Opinie:Nobelprijswinnende economie van klimaatverandering is misleidend en gevaarlijk, en hier is waarom Facebook negeert Brazilië-pagina's, profielen die nepnieuws verspreiden
Facebook negeert Brazilië-pagina's, profielen die nepnieuws verspreiden de relatie tussen fundamentele en afgeleide grootheden?
de relatie tussen fundamentele en afgeleide grootheden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

