
Wetenschap
De reden dat zuiver water als neutraal wordt beschouwd met betrekking tot de pH, omdat?
De reden dat zuiver water als pH-neutraal wordt beschouwd, is dat het een gelijke concentratie waterstofionen (H+) en hydroxide-ionen (OH-) heeft. De pH-schaal meet de zuurgraad of basiciteit van een oplossing op een schaal van 0 tot 14, waarbij 7 neutraal is. Wanneer de concentratie H+ ionen groter is dan de concentratie OH-ionen, is de oplossing zuur en heeft een pH-waarde lager dan 7. Omgekeerd, wanneer de concentratie OH-ionen groter is dan de concentratie H+ ionen, is de oplossing basisch en heeft een pH-waarde groter dan 7.
In het geval van zuiver water vindt auto-ionisatie van water plaats, een proces waarbij een watermolecuul zich splitst in H+ en OH-ionen. De evenwichtsconstante voor dit proces is erg klein, wat aangeeft dat de concentratie van H+ en OH-ionen in zuiver water erg laag is. Bij kamertemperatuur (25°C) bedraagt de concentratie H+ en OH-ionen in zuiver water ongeveer 1 x 10-7 mol per liter. Daarom ligt de pH van zuiver water zeer dicht bij 7, wat als neutraal wordt beschouwd.
 Lijst met basissen en zuren van huishoudens
Lijst met basissen en zuren van huishoudens Onderzoeksteam toont complexe, 3D-geprinte schwarzieten zijn bestand tegen druk wanneer ze zijn gecoat
Onderzoeksteam toont complexe, 3D-geprinte schwarzieten zijn bestand tegen druk wanneer ze zijn gecoat Natuurkundige identificeert hoe elektronenkristallen smelten
Natuurkundige identificeert hoe elektronenkristallen smelten  Welk chemisch proces scheidt metaal van gesteente?
Welk chemisch proces scheidt metaal van gesteente?  Waarom wordt de reageerbuis geel tijdens een elektrolysewaterexperiment?
Waarom wordt de reageerbuis geel tijdens een elektrolysewaterexperiment?
 Hoe thermische zonne-energie werkt
Hoe thermische zonne-energie werkt  Deeltjes aan het oceaanoppervlak en de zeebodem zijn niet zo verschillend
Deeltjes aan het oceaanoppervlak en de zeebodem zijn niet zo verschillend Eerste directe bewijs voor een mantelpluimoorsprong van Jurassic vloedbasalt in zuidelijk Afrika
Eerste directe bewijs voor een mantelpluimoorsprong van Jurassic vloedbasalt in zuidelijk Afrika Florida wacht:orkaan Dorian ziet er steeds grimmiger uit
Florida wacht:orkaan Dorian ziet er steeds grimmiger uit Werken aan groene groei in stedelijk China
Werken aan groene groei in stedelijk China
Hoofdlijnen
- Nieuwe inzichten over hoe de vogelgriep de soortbarrière overschrijdt
- Hebben planten rode bloedcellen?
- Zitten dieren vast in de tijd?
- Wetenschappers gebruiken geluidsgolven om te testen hoe goed synthetische antilichamen hun antigeendoelen binden
- De nadelen van gelelektroforese
- Waarom hebben kankercellen geen genetische meltdowns ondergaan?
- Waar zijn de virale genen voor?
- Hoe evolueren genomen tussen soorten? Team onderzoekt de sleutelrol van 3D-structuur in mannelijke geslachtscellen
- Onderzoekers onderzoeken hoe de eiwitfabrieken van een cel in elkaar worden gezet
- Een nieuwe aanwijzing voor een 50 jaar oud mysterie van stralingsschade
- VTT ontwikkelde een optische vezel van cellulose

- Onderzoekers die werken aan het terugwinnen van zeldzame aardelementen en het veiligstellen van kritieke materialen voor schone energietechnologieën

- Nieuwsgierige in elkaar grijpende moleculen vertonen een dubbele respons
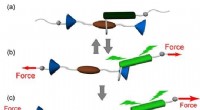
- Q&A:Op weg naar een nieuwe manier om zonnecellen te produceren
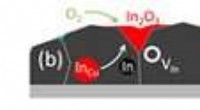
 Lye veilig gebruiken
Lye veilig gebruiken  Onderzoeksteam ontwikkelt nieuwe methode voor het bestuderen van atomaire structuren in materiaaloppervlakken
Onderzoeksteam ontwikkelt nieuwe methode voor het bestuderen van atomaire structuren in materiaaloppervlakken Digitaal slagveld doemt op voor de verkiezingen van 2020
Digitaal slagveld doemt op voor de verkiezingen van 2020 Vorticiteit reguleert golven in vloeistoffen
Vorticiteit reguleert golven in vloeistoffen Afbeelding:Door de hittebarrière
Afbeelding:Door de hittebarrière Terugroepacties voor voertuigveiligheid:waarom chauffeurs er geen acht op slaan
Terugroepacties voor voertuigveiligheid:waarom chauffeurs er geen acht op slaan  Slachtoffer-overlevenden van verkrachting voelen niet dat gerechtigheid is voldaan, zelfs als de beschuldigde naar de gevangenis gaat
Slachtoffer-overlevenden van verkrachting voelen niet dat gerechtigheid is voldaan, zelfs als de beschuldigde naar de gevangenis gaat Een aap en een virus:een miljoen jaar samen
Een aap en een virus:een miljoen jaar samen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

