
Wetenschap
Hoeveel covalente bindingen kan element X vormen?
1. Groepsnummer: Element X behoort tot een specifieke groep in het periodiek systeem, genummerd van 1 tot en met 18. Het groepsnummer geeft het aantal valentie-elektronen in de buitenste schil van X aan.
Als element X zich bijvoorbeeld in Groep 7 bevindt (ook bekend als de halogenen), heeft het zeven valentie-elektronen.
2. Valentie-elektronen: Valentie-elektronen zijn de elektronen in de buitenste schil van een atoom die deelnemen aan chemische bindingen. Het aantal valentie-elektronen bepaalt de chemische eigenschappen en het bindingsgedrag van het element.
In ons voorbeeld heeft element X zeven valentie-elektronen (als het zich in groep 7 bevindt).
3. Covalente obligaties: Covalente bindingen ontstaan wanneer atomen valentie-elektronen delen om een stabielere elektronenconfiguratie te bereiken. Elk gedeeld elektronenpaar wordt als één covalente binding beschouwd.
Daarom kan element X maximaal zeven covalente bindingen vormen als het al zijn zeven valentie-elektronen deelt met andere atomen.
Samenvattend wordt het aantal covalente bindingen dat een element X kan vormen bepaald door zijn valentie-elektronen. Element X kan covalente bindingen vormen die gelijk zijn aan het aantal valentie-elektronen dat het bezit. In het geval van een element uit Groep 7 kan het zeven covalente bindingen vormen.
 Een nieuwe katalysator voor energierijke aluminium-luchtstroombatterijen
Een nieuwe katalysator voor energierijke aluminium-luchtstroombatterijen Levende elektroden met bacteriën en organische elektronica
Levende elektroden met bacteriën en organische elektronica Gerecycleerde bureaustoelen omgetoverd tot hard-shell rugzakken en fietstassen
Gerecycleerde bureaustoelen omgetoverd tot hard-shell rugzakken en fietstassen Onderzoekers rapporteren hoogwaardige solid-state natrium-ionbatterij
Onderzoekers rapporteren hoogwaardige solid-state natrium-ionbatterij Is CH4 een ionisch of covalent molecuul?
Is CH4 een ionisch of covalent molecuul?
 Hoe mensen vogelgemeenschappen op eilanden transformeren
Hoe mensen vogelgemeenschappen op eilanden transformeren  Uitputting van het grondwater in de Amerikaanse High Plains leidt tot sombere vooruitzichten voor de graanproductie
Uitputting van het grondwater in de Amerikaanse High Plains leidt tot sombere vooruitzichten voor de graanproductie Greening the greyfields:hoe onze buitenwijken te vernieuwen voor meer leefbare, net-zero steden
Greening the greyfields:hoe onze buitenwijken te vernieuwen voor meer leefbare, net-zero steden Een beter begrip van hoe cirruswolken ontstaan
Een beter begrip van hoe cirruswolken ontstaan Uit modellering van de stedelijke groei blijkt dat steden zich op een manier ontwikkelen die vergelijkbaar is met kankertumoren
Uit modellering van de stedelijke groei blijkt dat steden zich op een manier ontwikkelen die vergelijkbaar is met kankertumoren
Hoofdlijnen
- Wat gebeurt er als we menselijke kwaliteiten toekennen aan bedrijven?
- Geen designerbaby’s, maar genbewerking om ziekten te voorkomen? Misschien
- Waarom stemmen mensen? Genetische variatie in politieke participatie
- Het belang van DNA-moleculen
- Cellulaire route zou bewijs kunnen leveren van hoe kanker en obesitas met elkaar verbonden zijn
- 'Vliegende vaccinator':kunnen genetisch gemanipuleerde muggen een nieuwe strategie tegen malaria bieden?
- Uit welke soorten moleculen bestaan RNA-moleculen?
- Vertakking voor voedsel:hoe voedingsstoffen de bloedsomloop van vliegen hervormen
- Twin Monkeys voor het eerst gekloond als Dolly the Sheep
- Thorium-aluminiumcomplex het eerste met een actinide-element dat elektronen afstaat bij binding met een metaal
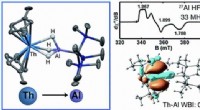
- Thorium-228-aanvoer rijp voor onderzoek naar medische toepassingen

- Nieuwe robotsensortechnologie kan reproductieve gezondheidsproblemen in realtime diagnosticeren

- Een Trojaanse paardenbenadering kan leiden tot behandelingen voor sommige antibioticaresistente bacteriën
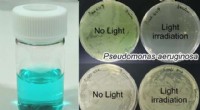
- Biologisch afbreekbare kunststoffen uit palmolieafval

 Sri Lanka zet zich schrap voor strandvervuiling als schip afbrandt
Sri Lanka zet zich schrap voor strandvervuiling als schip afbrandt Hoe een Afrikaanse vogel een betere waterfles zou kunnen inspireren
Hoe een Afrikaanse vogel een betere waterfles zou kunnen inspireren  Een algoritme om te detecteren wanneer online gesprekken waarschijnlijk lelijk worden
Een algoritme om te detecteren wanneer online gesprekken waarschijnlijk lelijk worden Team beschrijft MXene-ondersteunde PtCo-bimetaalkatalysator voor waterstofontwikkeling in zure omstandigheden
Team beschrijft MXene-ondersteunde PtCo-bimetaalkatalysator voor waterstofontwikkeling in zure omstandigheden  Hoe klein is een small-world netwerk?
Hoe klein is een small-world netwerk? Wetenschappers leggen voor het eerst een afbeelding vast van een elektronenbaan in een exciton
Wetenschappers leggen voor het eerst een afbeelding vast van een elektronenbaan in een exciton Het visualiseren van meerdere dimensies voor een grootbeeldanalyse van vleugelspanningen en prestaties
Het visualiseren van meerdere dimensies voor een grootbeeldanalyse van vleugelspanningen en prestaties Hoe beïnvloedt de afstand tussen Domino's de snelheid waarmee ze vallen?
Hoe beïnvloedt de afstand tussen Domino's de snelheid waarmee ze vallen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

