
Wetenschap
Wat is de sp3-gehybridiseerde structuur van SiF4?
Het siliciumatoom in SiF4 is sp3-gehybridiseerd. Dit betekent dat het siliciumatoom vier valentie-elektronen heeft, die allemaal worden gebruikt om vier enkele bindingen met de vier fluoratomen te vormen. De sp3-hybridisatie resulteert in de vorming van vier tetraëdrische orbitalen, die naar de hoeken van een tetraëder zijn gericht. De vier fluoratomen bezetten deze vier orbitalen en vormen de vier Si-F-bindingen.
De sp3-hybridisatie van het siliciumatoom in SiF4 is ook verantwoordelijk voor de tetraëdrische vorm van het molecuul. De vier tetraëdrische orbitalen wijzen in verschillende richtingen, en de vier fluoratomen zijn op de hoeken van een tetraëder geplaatst om afstoting tussen de elektronenparen te minimaliseren.
Samenvattend resulteert de sp3-gehybridiseerde structuur van SiF4 in een tetraëdrische moleculaire geometrie met vier Si-F-bindingen.
 Scienceweekprojecten van twee weken
Scienceweekprojecten van twee weken Om te zoemen of om te krabbelen? foeragerende bijen, dat is de vraag
Om te zoemen of om te krabbelen? foeragerende bijen, dat is de vraag  American River Basin Study vindt dat stijgende temperaturen het bekken in de rest van de 21e eeuw zullen beïnvloeden
American River Basin Study vindt dat stijgende temperaturen het bekken in de rest van de 21e eeuw zullen beïnvloeden Soorten fossielen en hoe ze zijn gevormd
Soorten fossielen en hoe ze zijn gevormd Tuinwormen en klimaatverandering ondermijnen natuurlijke kustbescherming
Tuinwormen en klimaatverandering ondermijnen natuurlijke kustbescherming
Hoofdlijnen
- Wat betekent generatietijd in de microbiologie?
- Wat zijn de componenten van nucleotiden?
- Studie:Hoe placenta's evolueerden bij zoogdieren
- Onderzoekers ontdekken hoe dieren hun puntige lichaamsdelen laten groeien
- Een bitter mysterie:wetenschappers sequencen 's werelds oudste plantengenoom van 6000 jaar oude watermeloenzaden
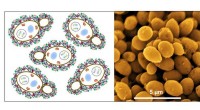
- Hoe het zien van de moleculaire machinerie van het coronavirus wetenschappers zal helpen een behandeling te ontwerpen
- Wat gebeurt er met de stikstof als organismen afsterven?
- Hoe cellen in de neus geuren detecteren
- Inheemse vissoorten lopen gevaar na verwijdering van water uit de Colorado-rivier
- Watersplitsingskatalysatoren ontwerpen met behulp van afvalgistbiomassa
- Een bionisch blad kan de wereld helpen voeden

- OLED's worden helderder en duurzamer

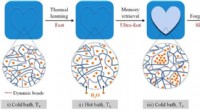
- Hydrogel bootst het menselijk brein na met het vermogen om te onthouden en te vergeten
- Twee-vogels-een-steen-strategie toont belofte in RNA-herhalende expansieziekten

 Thermostatische beweging:wat een rododendron ons kan leren over robotica
Thermostatische beweging:wat een rododendron ons kan leren over robotica Wat zijn de soorten wrijvingskracht?
Wat zijn de soorten wrijvingskracht?  Bedreigde planten in het Amazone-regenwoud
Bedreigde planten in het Amazone-regenwoud  Japanse aardbevingszone sterk beïnvloed door de effecten van wrijving
Japanse aardbevingszone sterk beïnvloed door de effecten van wrijving Intel en Softbank pas op. Open source komt naar de chipbusiness
Intel en Softbank pas op. Open source komt naar de chipbusiness NASA waarschuwde voor veiligheidsrisico's bij vertraagde lanceringen van privébemanningen (update)
NASA waarschuwde voor veiligheidsrisico's bij vertraagde lanceringen van privébemanningen (update) Hebben onderzoekers de ontbrekende schakel gevonden die het mysterieuze fenomeen verklaart dat bekend staat als sprookjescirkels?
Hebben onderzoekers de ontbrekende schakel gevonden die het mysterieuze fenomeen verklaart dat bekend staat als sprookjescirkels?  Afbeelding:Hubble-vingerafdrukken van een sterrenstelsel
Afbeelding:Hubble-vingerafdrukken van een sterrenstelsel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

