
Wetenschap
Kan argon een ionische binding vormen?
Argon kan geen ionische binding vormen omdat het een volledige valentieschil heeft en geen gedeeltelijke ladingen heeft die ionen met de tegenovergestelde lading zouden aantrekken. De gevulde elektronenschil maakt argon stabiel en niet bevorderlijk voor de vorming van de sterke elektrostatische aantrekkingskracht die kenmerkend is voor ionische binding. Ionische bindingen bestaan gewoonlijk tussen atomen met aanzienlijk verschillende elektronegativiteiten, waardoor elektronenoverdracht mogelijk is om tegengesteld geladen ionen te creëren, niet in niet-polaire elementen zoals argon.
 Wat ontstaat er als fenol reageert met ammoniumsulfiet in aanwezigheid van ammoniak?
Wat ontstaat er als fenol reageert met ammoniumsulfiet in aanwezigheid van ammoniak?  Wat is het twee-mixprincipe?
Wat is het twee-mixprincipe?  Team onthult katalysator die problematische CF-bindingen kan verbreken
Team onthult katalysator die problematische CF-bindingen kan verbreken Vooruitgang van elektrolyse bij hoge temperatuur:water splitsen om energie op te slaan als waterstof
Vooruitgang van elektrolyse bij hoge temperatuur:water splitsen om energie op te slaan als waterstof Hoe helpt het gas uit noppenfolie om iets dat erin zit te isoleren?
Hoe helpt het gas uit noppenfolie om iets dat erin zit te isoleren?
 "Diet of a Leaf Insect
"Diet of a Leaf Insect Energy Dept. biedt $ 2 miljard lening aan La. koolstofopslagproject
Energy Dept. biedt $ 2 miljard lening aan La. koolstofopslagproject Hoe wetenschappers drones gebruiken om het risico op catastrofale overstromingen van grote gletsjermeren te verkleinen
Hoe wetenschappers drones gebruiken om het risico op catastrofale overstromingen van grote gletsjermeren te verkleinen Hoe klimaatgrillen planten kunnen triggeren
Hoe klimaatgrillen planten kunnen triggeren  Mauritius ontwijkt tweede olielek terwijl brandstof uit het getroffen schip wordt gepompt
Mauritius ontwijkt tweede olielek terwijl brandstof uit het getroffen schip wordt gepompt
Hoofdlijnen
- leeuwen, chimpansees, haaien krijgen extra bescherming onder VN-verdrag
- Netwerken gebruiken om weefselspecifieke genregulatie te begrijpen
- Waarom is DNA-replicatie belangrijk voor de celdeling?
- GMO-experimenten
- Wat inktvisneuronen en een octopus in extase ons over onszelf kunnen leren
- Waarom verzamelen vrouwelijke grote hamerhaaien zich elke zomer in Frans-Polynesië?
- Een belangrijke reden waarom vrouwen stoppen met doctorale STEM-programma’s
- Hoeveel mitotische celdelingen zijn er nodig voordat één zygoot groeit in een organisme met 100 biljoen cellen?
- Het geheim van een lang leven? Vraag een geelbuikmarmot
- Nieuwe methode voor het produceren van synthetisch DNA
- Studie update etnobotanie, fytochemie en farmacologie van het geslacht Didymocarpus Wall.

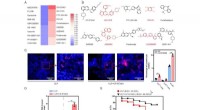
- PDGFR-kinaseremmer blijkt te beschermen tegen septische dood via regulering van BTLA
- Onderzoekers ontwikkelen verbeterd recyclingproces voor koolstofvezels

- Genetische schakelaars bij kanker nader bekijken

 3D-AFM-beelden simuleren voor systemen die niet in evenwicht zijn
3D-AFM-beelden simuleren voor systemen die niet in evenwicht zijn Wetenschappers ontwikkelen stereogedefinieerde N- en S-atoom-gecodeerde graphdiyne voor zuurstofevolutie
Wetenschappers ontwikkelen stereogedefinieerde N- en S-atoom-gecodeerde graphdiyne voor zuurstofevolutie Kan Twitter zijn 'kern' veranderen en Twitter blijven?
Kan Twitter zijn 'kern' veranderen en Twitter blijven?  Verschil tussen natriumcarbonaat en calciumcarbonaat
Verschil tussen natriumcarbonaat en calciumcarbonaat Onderzoekers combineren spintronica en nanofotonica in 2D-materiaal
Onderzoekers combineren spintronica en nanofotonica in 2D-materiaal Onderzoekers ontwikkelen methode voor synthese van DNA-geprogrammeerd materiaal
Onderzoekers ontwikkelen methode voor synthese van DNA-geprogrammeerd materiaal Calciumverbinding breekt zoals stoot als regel af
Calciumverbinding breekt zoals stoot als regel af Hoe vliegtuigen werken
Hoe vliegtuigen werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

