
Wetenschap
Kan een atoom meer dan één binding aangaan?
Atomen kunnen bindingen vormen met andere atomen door valentie-elektronen te delen of over te dragen. Wanneer atomen valentie-elektronen delen, vormen ze covalente bindingen. Wanneer atomen valentie-elektronen overbrengen, vormen ze ionische bindingen.
Het aantal bindingen dat een atoom kan maken, wordt beperkt door het aantal valentie-elektronen dat het heeft. Een atoom met één valentie-elektron kan bijvoorbeeld slechts één binding maken. Een atoom met twee valentie-elektronen kan twee bindingen maken. Een atoom met drie valentie-elektronen kan drie bindingen maken, enzovoort.
Sommige atomen kunnen ook meerdere bindingen vormen. Een meervoudige binding is een binding tussen twee atomen waarbij meer dan één paar elektronen betrokken zijn. Een dubbele binding is bijvoorbeeld een binding tussen twee atomen waarbij twee paren elektronen betrokken zijn. Een drievoudige binding is een binding tussen twee atomen waarbij drie elektronenparen betrokken zijn.
Het vermogen van een atoom om meerdere bindingen te vormen wordt bepaald door zijn atoomnummer. Het atoomnummer van een atoom is het aantal protonen in de kern van het atoom. Hoe hoger het atoomnummer van een atoom, hoe waarschijnlijker het is dat het meerdere bindingen kan vormen.
 Een fundamentele reactie in de organische chemie op zijn kop zetten - ontdekking van een nieuwe nucleofiele substitutiereactie
Een fundamentele reactie in de organische chemie op zijn kop zetten - ontdekking van een nieuwe nucleofiele substitutiereactie Worden stukjes droogijs kleiner door condensatie?
Worden stukjes droogijs kleiner door condensatie?  Samenwerking vormt de strategie voor het vasthouden van extracellulaire blaasjes
Samenwerking vormt de strategie voor het vasthouden van extracellulaire blaasjes Technologie verhoogt de output van microfluïdische onderzoeksgegevens 100-voudig
Technologie verhoogt de output van microfluïdische onderzoeksgegevens 100-voudig Schadelijke effecten van chloorgas
Schadelijke effecten van chloorgas
 Onderzoekers onderzoeken hoe mensen reageren op natuurbrandrook
Onderzoekers onderzoeken hoe mensen reageren op natuurbrandrook Hoe psychologie mensen kan helpen een klimaatvriendelijker leven te leiden – lessen van over de hele wereld
Hoe psychologie mensen kan helpen een klimaatvriendelijker leven te leiden – lessen van over de hele wereld  NASA-ballonmissie legt elektrisch blauwe wolken vast
NASA-ballonmissie legt elektrisch blauwe wolken vast Nieuw onderzoek in Kenia vindt een goede plek voor het oogsten van rifvissen
Nieuw onderzoek in Kenia vindt een goede plek voor het oogsten van rifvissen Afname uitstoot lockdown heeft geen effect op klimaat
Afname uitstoot lockdown heeft geen effect op klimaat
Hoofdlijnen
- Uit onderzoek blijkt hoe de adelborstvis zijn urenlange paringsroep volhoudt
- In de ruimte gekweekte vliegen vertonen een verzwakte immuniteit tegen schimmels
- Wetenschappers rangschikken 's werelds grootste pangenoom om genetische mysteries achter fijnere zijde te helpen ontrafelen
- Zebravisembryo's helpen bewijzen wat er met nanodeeltjes in het bloed gebeurt
- Voelen planten pijn?
- Nieuwe studie over pathogene Leishmania-parasiet werpt licht op de evolutie van celkrachtproducerende machines
- Fotograaf legt menselijk gezicht van bedreigde diersoorten vast
- Infecteert COVID-19 wilde dieren? We testen soorten, van vleermuizen tot zeehonden, om erachter te komen
- Waarom bestaan er wetenschappelijke modellen?
- Veranderingen in suikerachtige moleculen aan het oppervlak helpen kanker uitzaaien

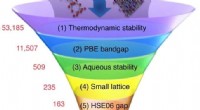
- Uitgebreide elektronische structuurmethoden voor materiaalontwerp
- De scheikundige laat zien dat intermoleculaire interacties voorheen onbekende dimensies kunnen bereiken

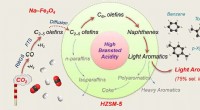
- Onderzoekers synthetiseren lichte aromaten uit kooldioxidehydrogenering
- Onderzoekers ontwikkelen nieuwe strategie voor efficiënte OLED-schermen met actieve matrix

 Wetenschappers bevestigen een structurele overeenkomst gevonden in zowel menselijke cellen als neutronensterren
Wetenschappers bevestigen een structurele overeenkomst gevonden in zowel menselijke cellen als neutronensterren Hawaii-vulkaan ontketent meer kleine explosies, kronkelende lava
Hawaii-vulkaan ontketent meer kleine explosies, kronkelende lava Wetenschappers zetten een stap voorwaarts in het begrijpen hoe patiënten met chronische infecties met cystische fibrose kunnen worden aangepakt
Wetenschappers zetten een stap voorwaarts in het begrijpen hoe patiënten met chronische infecties met cystische fibrose kunnen worden aangepakt  Onderzoekers verhogen de temperatuur voor excitoncondensatie
Onderzoekers verhogen de temperatuur voor excitoncondensatie Wat is het proces waarbij water uit het blad ontsnapt?
Wat is het proces waarbij water uit het blad ontsnapt?  Payne-Gaposchkin,
Payne-Gaposchkin,  Hoe zonnewarmte ervoor zorgt dat delen van de grootste ijsplaat van Antarctica snel smelten
Hoe zonnewarmte ervoor zorgt dat delen van de grootste ijsplaat van Antarctica snel smelten Boeren hebben de meest dodelijke baan van Groot-Brittannië - hier kun je ze veiliger maken
Boeren hebben de meest dodelijke baan van Groot-Brittannië - hier kun je ze veiliger maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

