
Wetenschap
Welke moleculaire vaste stoffen hebben het hoogste smeltpunt?
Diamant heeft het hoogste smeltpunt onder de moleculaire vaste stoffen. Diamant bestaat uit koolstofatomen die in een stijve, driedimensionale roosterstructuur zijn gerangschikt en zo een gigantisch covalent netwerk vormen. De sterke covalente bindingen tussen de koolstofatomen in diamant resulteren in een uitzonderlijke hardheid en een hoog smeltpunt. Het smeltpunt van diamant is ongeveer 3.550 graden Celsius (6.442 graden Fahrenheit) bij atmosferische druk. Daarentegen hebben andere moleculaire vaste stoffen, zoals waterijs of vast koolstofdioxide (droogijs), veel lagere smeltpunten als gevolg van zwakkere intermoleculaire krachten.
 Een nieuwe methode om ionen door celmembranen te transporteren op basis van een enkel aminozuur
Een nieuwe methode om ionen door celmembranen te transporteren op basis van een enkel aminozuur Een revolutionair materiaal voor ruimtevaart en neuromorfisch computergebruik
Een revolutionair materiaal voor ruimtevaart en neuromorfisch computergebruik Onderzoekers ontwikkelen synthetische T-cellen die de vorm nabootsen, functie van menselijke versie
Onderzoekers ontwikkelen synthetische T-cellen die de vorm nabootsen, functie van menselijke versie Wetenschappers ontwikkelen een goedkopere methode die kan helpen bij het maken van brandstoffen uit planten
Wetenschappers ontwikkelen een goedkopere methode die kan helpen bij het maken van brandstoffen uit planten Video:De enige detox die je ooit nodig zult hebben
Video:De enige detox die je ooit nodig zult hebben
Hoofdlijnen
- Nieuw genomisch onderzoek biedt een glimp van hoe walvissen zich kunnen aanpassen aan de oceaan
- Wetenschappers krijgen een nieuw inzicht in het herstelproces van nucleotide-excisie
- Kunnen katten en coyotes naast elkaar bestaan?
- Hoe stamcellen van planten zichzelf vernieuwen:een cytokinineverhaal
- Wat is jaloezie? Hoe verschilt jaloezie van afgunst?
- Wat is de definitie van toegevoegde suiker?
- Planten kunnen kiezen tussen alternatieve reacties op concurrentie
- Zijn mensen het slimste dier?
- Onderzoekers concentreren zich op de manier waarop bacteriën voedselvergiftiging veroorzaken
- Wetenschappers vinden goedkopere manier om waterstof uit water te maken

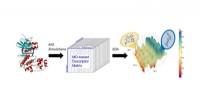
- Moleculaire dynamiek, machine learning maakt hypervoorspellende computermodellen
- De deeltjesfasechemie zorgt ervoor dat roet beter wolken kan zaaien
- Multisample-techniek om celadhesie te analyseren
- Zeemosselen zijn een model voor het verbeteren van kracht, rekbaarheid en hechting in hydrogels voor wondgenezing

 Wereldsnelheidsrecord voor polymeersimulaties meer dan honderdvoudig verbrijzeld
Wereldsnelheidsrecord voor polymeersimulaties meer dan honderdvoudig verbrijzeld Een nieuwe kijk op ongeordende koolstof
Een nieuwe kijk op ongeordende koolstof Het effect van bevriezen en ontdooien op rots
Het effect van bevriezen en ontdooien op rots  Wat biologen nog steeds niet weten over bioluminescentie
Wat biologen nog steeds niet weten over bioluminescentie  de Maya's Is de beschaving geëindigd vanwege de klimaatverandering?
de Maya's Is de beschaving geëindigd vanwege de klimaatverandering?  Luchtvaartmaatschappijen in het Midden-Oosten verliezen $ 7 miljard omdat luchthavens gesloten zijn om het virus te bestrijden
Luchtvaartmaatschappijen in het Midden-Oosten verliezen $ 7 miljard omdat luchthavens gesloten zijn om het virus te bestrijden Strategie voor het evalueren van de energieprestaties van op metaal-organische-framework gebaseerde kooldioxide-adsorbentia
Strategie voor het evalueren van de energieprestaties van op metaal-organische-framework gebaseerde kooldioxide-adsorbentia Een magnetisch veld gebruiken om de lucht-waterinterface op afstand te bedienen
Een magnetisch veld gebruiken om de lucht-waterinterface op afstand te bedienen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

