
Wetenschap
Welke massa waterstofchloride is nodig om te reageren met 100 g roest?
Roest bestaat voornamelijk uit ijzeroxide, dat de chemische formule Fe2O3 heeft. De reactie tussen ijzeroxide en waterstofchloride kan als volgt worden weergegeven:
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Uit deze vergelijking kunnen we afleiden dat er 6 mol HCl nodig is om te reageren met 1 mol Fe2O3. Om het aantal mol Fe2O3 aanwezig in 100 g roest te berekenen, moeten we de roestmassa delen door de molaire massa van Fe2O3 (159,69 g/mol):
Mol Fe2O3 =100 g / 159,69 g/mol =0,626 mol
Omdat er voor elke mol Fe2O3 6 mol HCl nodig is, is het aantal mol HCl dat nodig is om te reageren met 0,626 mol Fe2O3:
Mol HCl =6 mol HCl / 1 mol Fe2O3 × 0,626 mol Fe2O3 =3,756 mol
Ten slotte kunnen we het aantal mol HCl weer omrekenen naar grammen met behulp van de molaire massa van HCl (36,46 g/mol):
Massa HCl =3,756 mol HCl x 36,46 g/mol =137,2 g
Daarom is er 137,2 gram waterstofchloride nodig om te reageren met 100 gram roest.
 Vulkaanuitbarstingen veroorzaakten direct oceaanverzuring tijdens het vroege Krijt
Vulkaanuitbarstingen veroorzaakten direct oceaanverzuring tijdens het vroege Krijt Satellietbeelden in uw achtertuin vastleggen en bijdragen aan een momentopname van de klimaatcrisis
Satellietbeelden in uw achtertuin vastleggen en bijdragen aan een momentopname van de klimaatcrisis Les geleerd, en sommigen onopgemerkt, na orkanen
Les geleerd, en sommigen onopgemerkt, na orkanen Uit langetermijnonderzoek blijkt hoe klimaatverandering zich afspeelt in echte ecosystemen
Uit langetermijnonderzoek blijkt hoe klimaatverandering zich afspeelt in echte ecosystemen  Nieuw project onderzoekt hoe op duurzamere manieren aan de verwachtingen voor bossen kan worden voldaan
Nieuw project onderzoekt hoe op duurzamere manieren aan de verwachtingen voor bossen kan worden voldaan
Hoofdlijnen
- Hoe de microprocessor de miRNA-productie nauwkeurig initieert
- 30 miljoen jaar oude amfibische beverfossiel is oudste ooit gevonden
- Experiment laat zien hoe wormgastheren en het bijbehorende microbioom gezamenlijk bijdragen aan aanpassing aan het milieu
- Waarom is fotosynthese belangrijk voor mensen?
- Reconstructies laten zien hoe enkele van de vroegste dieren leefden en stierven (met video)
- Simpele microscoopexperimenten
- Het voortbestaan van de bedreigde monarchvlinder hangt af van instandhouding buiten de grenzen
- Hoe worden restrictie-enzymen gebruikt in de biotechnologie?
- Lijst met ingekapselde bacteriën
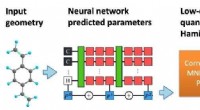
- Doorbraak gemeld in door machine learning verbeterde kwantumchemie
- Druk zorgt voor de beste koeling

- Nieuwe verbindingen uit de zeester van het Kuril-bekken tonen werkzaamheid tegen kankercellen.

- Handdesinfecterend middel opnieuw ontwerpen en doneren 7, 000 gallons om COVID-19 te bestrijden

- Dicht en permeabel:moleculaire organisatie van nauwe kruispunten gedecodeerd
 Hoe een ecosysteem in een fles met vissen en planten te maken
Hoe een ecosysteem in een fles met vissen en planten te maken De winst van Samsung zakt meer dan de helft naarmate de chipmarkt verzwakt
De winst van Samsung zakt meer dan de helft naarmate de chipmarkt verzwakt Wat is een draaimachine?
Wat is een draaimachine?  Hoe bacteriën hun onzichtbaarheidsmantels hechten aan de immuunafweer
Hoe bacteriën hun onzichtbaarheidsmantels hechten aan de immuunafweer  In het laboratorium gekweekt vlees zou de mensheid een ernstig moreel falen kunnen laten negeren
In het laboratorium gekweekt vlees zou de mensheid een ernstig moreel falen kunnen laten negeren De helft van de onderzoekers maakt zich zorgen over de langetermijneffecten van COVID-19 op de financiering – wereldwijde studie
De helft van de onderzoekers maakt zich zorgen over de langetermijneffecten van COVID-19 op de financiering – wereldwijde studie Nanomateriaal van een nieuwe klasse
Nanomateriaal van een nieuwe klasse Ondergronds neutrino-experiment vormt de basis voor diepgaande ontdekkingen over materie
Ondergronds neutrino-experiment vormt de basis voor diepgaande ontdekkingen over materie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

