
Wetenschap
Hoe kan zout de kooktijd van water beïnvloeden?
1. Kookpunthoogte: Wanneer u een opgeloste stof (zoals zout) oplost in een oplosmiddel (zoals water), neemt het kookpunt van de oplossing toe. Dit betekent dat het water met opgelost zout een hogere temperatuur nodig heeft om te koken dan zuiver water. De kookpuntverhoging is recht evenredig met de hoeveelheid aanwezige opgeloste stof. Dus hoe meer zout je toevoegt, hoe hoger het kookpunt zal zijn en hoe langer het duurt voordat het water kookt.
De kookpuntverhoging veroorzaakt door zout is relatief klein in vergelijking met andere opgeloste stoffen, maar is nog steeds merkbaar. Het toevoegen van 1 gram zout aan 100 gram water verhoogt bijvoorbeeld het kookpunt met ongeveer 0,05 graden Celsius.
2. Oppervlaktespanning: Zout kan ook de oppervlaktespanning van water beïnvloeden. Oppervlaktespanning is de kracht die ervoor zorgt dat de moleculen aan het oppervlak van een vloeistof naar binnen worden getrokken, waardoor een soort ‘huid’ op het oppervlak ontstaat. Zout verlaagt de oppervlaktespanning van water. Wanneer water kookt, vormen zich stoombellen die naar de oppervlakte stijgen. Met een lagere oppervlaktespanning kunnen de belletjes gemakkelijker ontsnappen, wat leidt tot een iets sneller kookproces.
Het effect van zout op de oppervlaktespanning van water is relatief klein en heeft een kleine invloed op de kooktijd.
Kortom, zout verlengt over het algemeen de kooktijd van water door het kookpunt te verhogen. De omvang van dit effect is echter klein en andere factoren zoals hoogte en atmosferische druk kunnen een grotere invloed hebben op de kooktijd.
 Nieuw Griekenland brand uitbreekt, aanzetten tot evacuaties
Nieuw Griekenland brand uitbreekt, aanzetten tot evacuaties Onderzoekers leggen uit hoe steden ecologisch duurzame verdichting kunnen implementeren
Onderzoekers leggen uit hoe steden ecologisch duurzame verdichting kunnen implementeren  Geo-engineering, andere technologieën zullen klimaatproblemen niet oplossen
Geo-engineering, andere technologieën zullen klimaatproblemen niet oplossen Textiel dat zich ontwikkelt om aan de vraag naar duurzame materialen te voldoen
Textiel dat zich ontwikkelt om aan de vraag naar duurzame materialen te voldoen De 10 belangrijkste oorzaken van opwarming van de aarde
De 10 belangrijkste oorzaken van opwarming van de aarde
Hoofdlijnen
- Je telefoon is een kiemfabriek, dus stop ermee om hem naar het toilet te brengen
- Maïsplaag maakt gebruik van plantafweerstoffen om zichzelf te beschermen
- De chemische samenstelling van voedingsstoffen Agar
- Wat is een diatomische reactie?
- Hoe houdt evolutie het creationisme in?
- Hoe bijen beslissen wat ze moeten zijn:Onderzoekers koppelen omkeerbare 'epigenetische' gedragspatronen
- Heeft het herschikken van chromosomen invloed op hun functie?
- Welke soorten genen hebben plasmiden?
- Onderzoeker ontdekt dat houtkikkers snel evolueerden als reactie op strooizout
- Nieuw begrip van hoe cellen tunnels vormen, kan helpen bij het behandelen van wonden, tumoren

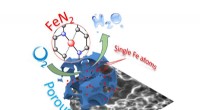
- Katalysatorvooruitgang kan leiden tot zuinige brandstofcellen
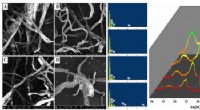
- Wetenschappers rapporteren efficiënt gebruik van oud papier voor de productie van cellulase door Trichoderma longiflorum
- Dragende verstrikkingen in polymeerglazen

- Hoe computers op zoek zijn naar drugs van de toekomst

 Het begin van de rotatie van sterrenstelsels in het vroege heelal vastleggen
Het begin van de rotatie van sterrenstelsels in het vroege heelal vastleggen Waar komen de kosmische straling met de hoogste energie vandaan? Niet door gammaflitsen, zegt IceCube-onderzoek
Waar komen de kosmische straling met de hoogste energie vandaan? Niet door gammaflitsen, zegt IceCube-onderzoek  Hoe planten evolueerden om de kou te weerstaan
Hoe planten evolueerden om de kou te weerstaan  Afbeelding:berg Fuji, Japan
Afbeelding:berg Fuji, Japan Onderzoekers vinden dat het nieuwe algoritme voor congestiecontrole van Google gegevens niet eerlijk behandelt
Onderzoekers vinden dat het nieuwe algoritme voor congestiecontrole van Google gegevens niet eerlijk behandelt NRL-wetenschappers verhogen de paraatheid van oorlogsvechters tegen onzichtbare bedreigingen
NRL-wetenschappers verhogen de paraatheid van oorlogsvechters tegen onzichtbare bedreigingen Steden met een hoge dichtheid zijn economisch gunstig, maar leiden tot grotere ongelijkheid
Steden met een hoge dichtheid zijn economisch gunstig, maar leiden tot grotere ongelijkheid Martian Ridge brengt rovers kleurtalenten naar voren
Martian Ridge brengt rovers kleurtalenten naar voren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

