
Wetenschap
Zit waterstof in zijn eigen groep?
Waterstof bevindt zich in zijn eigen groep op het periodiek systeem, Groep 1, ook wel de waterstofgroep genoemd. Dit komt omdat waterstof unieke eigenschappen heeft die het onderscheiden van de andere elementen in het periodiek systeem.
Hoewel waterstof één valentie-elektron heeft, zoals de alkalimetalen in groep 1, is het chemische gedrag ervan heel anders. Waterstof kan bijvoorbeeld covalente bindingen vormen met niet-metalen, terwijl alkalimetalen uitsluitend ionische bindingen vormen. Bovendien heeft waterstof een zeer lage atoommassa en een hoge ionisatie-energie, waardoor het zich onderscheidt van andere elementen in Groep 1.
Daarom wordt waterstof in zijn eigen groep geplaatst om de unieke kenmerken ervan te erkennen en om te weerspiegelen dat het niet netjes in een andere groep past.
 Wat gebeurt er met ionische en covalente verbindingen als ze in water worden opgelost?
Wat gebeurt er met ionische en covalente verbindingen als ze in water worden opgelost?  Hoe preprints de wetenschapscommunicatie tijdens de pandemie versnelden
Hoe preprints de wetenschapscommunicatie tijdens de pandemie versnelden  Antibiotica leren om effectievere moordenaars te zijn
Antibiotica leren om effectievere moordenaars te zijn Hoe Natrium Chloriet
Hoe Natrium Chloriet Sommige bestaande geneesmiddelen tegen kanker kunnen gedeeltelijk werken door zich te richten op RNA, studie toont
Sommige bestaande geneesmiddelen tegen kanker kunnen gedeeltelijk werken door zich te richten op RNA, studie toont
 Onverwachte resultaten:schade aan Puerto Ricaanse koffieplantages door orkaan Maria gevarieerd
Onverwachte resultaten:schade aan Puerto Ricaanse koffieplantages door orkaan Maria gevarieerd Om klimaatverandering tegen te gaan, wetenschap moet worden gemobiliseerd zoals het was in de Tweede Wereldoorlog
Om klimaatverandering tegen te gaan, wetenschap moet worden gemobiliseerd zoals het was in de Tweede Wereldoorlog Schattingen van recreatief gebruikswaarden kunnen gedurende tientallen jaren stabiel blijven
Schattingen van recreatief gebruikswaarden kunnen gedurende tientallen jaren stabiel blijven Wetenschappers vinden waarschijnlijke bron van methaan op Mars
Wetenschappers vinden waarschijnlijke bron van methaan op Mars Dodental van overstromingen in Henan stijgt tot 71 terwijl China zich schrap zet voor meer regen
Dodental van overstromingen in Henan stijgt tot 71 terwijl China zich schrap zet voor meer regen
Hoofdlijnen
- In welke drie informele groepen kunnen schimmels worden onderverdeeld?
- Wat is maïsplastic?
- Onderzoekers ontdekken hoe cellen virustoxine herkennen
- Beweging van DNA gekoppeld aan de reactie op schade, het vermogen om zichzelf te herstellen
- Seks:waarom moeite doen? Wetenschappers onderzoeken evolutionaire mysteries
- Wetenschappers gebruiken een supercomputer om te leren hoe cicadevleugels bacteriën doden
- Wetenschappers manipuleren de Set2-route om te laten zien hoe genen getrouw worden gekopieerd
- Hoe de verkeerde genen worden onderdrukt
- Actine-onderzoek laat zien hoe vlindervleugels hun levendige kleuren krijgen
- Nieuwe materialen met een hoge zuurstof-ionengeleiding die een duurzame toekomst opent
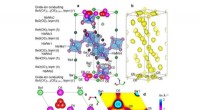
- Een nieuwe strategie om koolstofnitride-fotokatalysatoren voor stikstofreductie te stabiliseren

- Klaar voor de zomerzon met groene zonneschermen
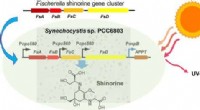
- Waterstof brandstofcellen:Met een database van 500, 000 materialen, onderzoekers kijken naar de beste weddenschappen

- In een veld waar kleiner beter is, onderzoekers ontdekken 's werelds kleinste antistoffen
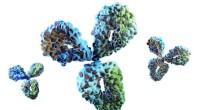
 10 luchtvaartinnovaties die zonder op de grond blijven zitten
10 luchtvaartinnovaties die zonder op de grond blijven zitten  Topologische nano-elektronica
Topologische nano-elektronica Alpaca's bleken het enige zoogdier te zijn dat rechtstreeks de baarmoeder insemineerde
Alpaca's bleken het enige zoogdier te zijn dat rechtstreeks de baarmoeder insemineerde  Hoeveel tijd is één dag op Mars?
Hoeveel tijd is één dag op Mars?  Onderzoekers volgen evolutie van zelfbeheersing
Onderzoekers volgen evolutie van zelfbeheersing Het belang van Boyles Gas Law in het dagelijks leven
Het belang van Boyles Gas Law in het dagelijks leven Hoe beïnvloedt erosie de aarde?
Hoe beïnvloedt erosie de aarde?  Nieuw elektronisch papier geeft schitterende kleuren weer
Nieuw elektronisch papier geeft schitterende kleuren weer
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

