
Wetenschap
Hoeveel moleculen zitten er in een monster van 4,15 g dimethylkwik?
De molaire massa van dimethylkwik (CH3)2Hg is de som van de atoommassa's van de samenstellende atomen:2(12,01 g/mol) voor de twee koolstofatomen, 6(1,01 g/mol) voor de zes waterstofatomen en 1( 200,59 g/mol) voor het kwikatoom. Daarom is de molaire massa van dimethylkwik ongeveer 230,64 g/mol.
Nu kunnen we de gegeven massa dimethylkwik (4,15 g) en zijn molaire massa gebruiken om het aantal mol in het monster te bepalen:
Mol dimethylkwik =massa / molaire massa
Mol dimethylkwik =4,15 g / 230,64 g/mol
Mol dimethylkwik ≈ 0,0180 mol
Ten slotte kunnen we het aantal mol dimethylkwik vermenigvuldigen met het getal van Avogadro om het aantal moleculen in het monster te vinden:
Aantal moleculen =Mol × getal van Avogadro
Aantal moleculen ≈ 0,0180 mol × 6,022 x 10^23 moleculen/mol
Aantal moleculen ≈ 1,08 x 10^23 moleculen
Daarom bevat een monster van 4,15 gram dimethylkwik ongeveer 1,08 x 10^23 moleculen.
 Wetenschappers ontdekken hoe we zure smaak detecteren
Wetenschappers ontdekken hoe we zure smaak detecteren  Wat is de ionische verbinding voor K2O?
Wat is de ionische verbinding voor K2O?  Het blootleggen van bacteriële celwandgeheimen om antibioticaresistentie te bestrijden
Het blootleggen van bacteriële celwandgeheimen om antibioticaresistentie te bestrijden Word wakker en ruik de koffie:onderzoek toont aan dat bevriezing van bonen het aroma kan behouden
Word wakker en ruik de koffie:onderzoek toont aan dat bevriezing van bonen het aroma kan behouden cel gedrag, ooit gehuld in mysterie, wordt geopenbaard in een nieuw licht
cel gedrag, ooit gehuld in mysterie, wordt geopenbaard in een nieuw licht
Hoofdlijnen
- Lichaamssystemen en hun functies
- G2-fase: wat gebeurt er in deze subfase van de celcyclus?
- DNA wordt vaak gebruikt bij het oplossen van misdaden. Maar hoe werkt profilering eigenlijk?
- Uit onderzoek blijkt dat oesters door middel van filtratie kunnen helpen het rif schoon te maken
- Noordelijke blootstelling:fossielen van een zuidelijke walvis voor het eerst gevonden in het noorden
- Onderzoekers ontdekken details over hoe bacteriën beschermende barrières bouwen, wat nieuwe antibiotica kan opleveren
- Hoe zorgt heet water ervoor dat DNA vrijkomt in de celkernen?
- Waarom liegen we?
- Hoe zijn sterk gevouwen membranen een voordeel voor de functies van cellulaire delen?
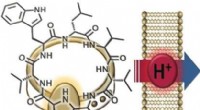
- Chemische synthese toont aan dat antibioticum uit de menselijke neus werkt door protontranslocatie
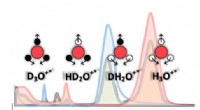
- Vloeibaar water is meer dan alleen waterstof-zuurstofmoleculen
- Door elektriciteit aangedreven onderzeese reacties kunnen belangrijk zijn geweest voor het ontstaan van leven

- Vorming van goudbindingen in realtime gevolgd met behulp van nieuwe moleculaire spectroscopietechniek

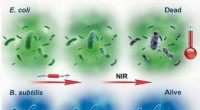
- Selectieve fotothermische therapie met supramoleculaire radicale anionen die in situ worden gegenereerd
 Voltooiing van de informatiekaart over aardbevingen in Oost-Azië en vulkanische gevaren
Voltooiing van de informatiekaart over aardbevingen in Oost-Azië en vulkanische gevaren Hoe verbinden de luchtruimten in het sponsachtige mesofyl zich met de buitenkant van het blad?
Hoe verbinden de luchtruimten in het sponsachtige mesofyl zich met de buitenkant van het blad?  De houding van Amerikanen over wapens beïnvloed door ras en geslacht van eigenaren
De houding van Amerikanen over wapens beïnvloed door ras en geslacht van eigenaren De rook van natuurbranden treft de inheemse gemeenschappen in Californië onevenredig zwaar, zo blijkt uit nieuw onderzoek
De rook van natuurbranden treft de inheemse gemeenschappen in Californië onevenredig zwaar, zo blijkt uit nieuw onderzoek  NASA's volgende Mars-missie om het interieur van de Rode Planeet te onderzoeken
NASA's volgende Mars-missie om het interieur van de Rode Planeet te onderzoeken Voorbij de grenzen van conventionele elektronica:stabiele organische moleculaire nanodraden
Voorbij de grenzen van conventionele elektronica:stabiele organische moleculaire nanodraden Doorbraak in microproductie is bedraad voor geluid
Doorbraak in microproductie is bedraad voor geluid Controle van het zeolietporiëninterieur voor chemo-selectieve alkyn/olefinescheidingen
Controle van het zeolietporiëninterieur voor chemo-selectieve alkyn/olefinescheidingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

