
Wetenschap
Wat is deze empirische formule - C5H8NO4?
1. Converteer de percentages naar grammen:
- Koolstof:52,17% =52,17 g
- Waterstof:6,90% =6,90 g
- Stikstof:9,52% =9,52 g
- Zuurstof:31,41% =31,41 g
2. Converteer de grammen van elk element naar mol:
- Koolstof:52,17 g / 12,01 g/mol =4,34 mol
- Waterstof:6,90 g / 1,01 g/mol =6,84 mol
- Stikstof:9,52 g / 14,01 g/mol =0,68 mol
- Zuurstof:31,41 g / 16,00 g/mol =1,96 mol
3. Deel elke molwaarde door de kleinste molwaarde om de eenvoudigste gehele getalsverhouding te krijgen:
- Koolstof:4,34 mol / 0,68 mol ≈ 6,4
- Waterstof:6,84 mol / 0,68 mol ≈ 10,1
- Stikstof:0,68 mol / 0,68 mol =1
- Zuurstof:1,96 mol / 0,68 mol ≈ 2,9
4. Rond de verhoudingen af op de dichtstbijzijnde gehele getallen:
- Koolstof:6
- Waterstof:10
- Stikstof:1
- Zuurstof:3
5. Schrijf de empirische formule met behulp van de afgeronde verhoudingen:
C6H10NO3
 NASA vindt tropische depressie Peipah aan het verdwijnen
NASA vindt tropische depressie Peipah aan het verdwijnen Feiten over Baby Cougars
Feiten over Baby Cougars Meerjarig onderzoek in onderzeeër-canyon daagt leerboektheorieën over troebelheidsstromen uit
Meerjarig onderzoek in onderzeeër-canyon daagt leerboektheorieën over troebelheidsstromen uit Onze bijen lopen nog steeds risico - Hier is hoe u hen kunt helpen
Onze bijen lopen nog steeds risico - Hier is hoe u hen kunt helpen Een snelle transitie van de energiesystemen van de wereld
Een snelle transitie van de energiesystemen van de wereld
Hoofdlijnen
- Springgenen werpen licht op hoe geavanceerd leven mogelijk is ontstaan
- Wat doen de cilia en flagellen in een cel?
- Welke moleculen worden verwerkt door het ruwe endoplasmatisch reticulum (ER)?
- Hoe reageren cellen op micro- en nanoplastics?
- Babywitte haaien zijn het liefst dichter bij de kust, ontdekken wetenschappers
- Zes belangrijkste celfuncties
- In het ei leren Amerikaanse brulkikkers hoe ze kunnen voorkomen dat ze een lunch worden
- Zou een blad functioneren als een orgaansysteem of weefsel om voedsel voor de plant te maken?
- Genetische modificatie en genoombewerking zijn afhankelijk van actieve rollen voor onderzoekers en de industrie
- Forensische wetenschappers herstellen menselijk DNA van muggen

- Synthetisch rubber presteert beter dan natuurlijk rubber

- Polymeercoating koelt gebouwen af

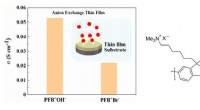
- De eerste geleidbaarheid van hydroxide in dunne films van aniongeleidende polymeren
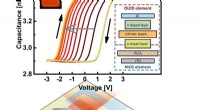
- pinMOS:nieuw geheugenapparaat kan optisch of elektrisch worden beschreven en uitgelezen
 Onderzoekers vinden 3, 000 jaar oud slachtoffer van haaienaanval
Onderzoekers vinden 3, 000 jaar oud slachtoffer van haaienaanval Onderzoekers ontdekken dat sommige cidermakers onnodige suiker toevoegen
Onderzoekers ontdekken dat sommige cidermakers onnodige suiker toevoegen Hoe de straal te vinden
Hoe de straal te vinden  Dynamisch poortproces waargenomen met een snelheid van minder dan 2 nm in nanokanalen
Dynamisch poortproces waargenomen met een snelheid van minder dan 2 nm in nanokanalen Fotonen (kwantisatie): definitie, eigenschappen en golf-deeltje dualiteit
Fotonen (kwantisatie): definitie, eigenschappen en golf-deeltje dualiteit  Strijd tussen Trump en staten over autovervuiling leidt tot rechtbank
Strijd tussen Trump en staten over autovervuiling leidt tot rechtbank Het vreemde geval van de duikvlieg
Het vreemde geval van de duikvlieg Kunstmatige hersennetwerken gesimuleerd met nieuwe kwantummaterialen
Kunstmatige hersennetwerken gesimuleerd met nieuwe kwantummaterialen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

