
Wetenschap
Waarom verliest natrium een elektron en krijgt het 1 lading?
De reden waarom natrium zijn buitenste elektron verliest, is omdat het niet erg sterk door de kern wordt aangetrokken. Dit komt omdat het buitenste elektron ver van de kern verwijderd is en de aantrekkingskracht tussen de kern en het elektron afneemt naarmate de afstand daartussen groter wordt. Bovendien wordt het buitenste elektron afgeschermd van de kern door de andere elektronen in het atoom. Dit afschermende effect vermindert ook de aantrekkingskracht tussen de kern en het buitenste elektron.
Als gevolg van deze factoren wordt het buitenste elektron van natrium zwak vastgehouden en kan het gemakkelijk uit het atoom worden verwijderd. Wanneer natrium dit elektron verliest, wordt het positief geladen omdat het nu één proton meer heeft dan een elektron.
 Onderzoek naar de voordelen van defecten in lasergefabriceerde materialen
Onderzoek naar de voordelen van defecten in lasergefabriceerde materialen Stimuleren van PET-recycling met hogere normen voor laboratoriumexperimenten
Stimuleren van PET-recycling met hogere normen voor laboratoriumexperimenten  Symmetrische splitsing van disulfiden is snel en biocompatibel
Symmetrische splitsing van disulfiden is snel en biocompatibel Waarom ijspegels golven
Waarom ijspegels golven  Eerste contact tussen malaria en mens in kaart gebracht met Nobelprijswinnende technologie
Eerste contact tussen malaria en mens in kaart gebracht met Nobelprijswinnende technologie
 Winterijs op meren, rivieren en vijvers:verleden tijd?
Winterijs op meren, rivieren en vijvers:verleden tijd?  Wetenschappers gebruiken sociale media (vakantiefoto's van Flickr) om te bestuderen hoe mensen natuurgebieden gebruiken voor toerisme
Wetenschappers gebruiken sociale media (vakantiefoto's van Flickr) om te bestuderen hoe mensen natuurgebieden gebruiken voor toerisme  Waarom voedingskeuzes een impact hebben op de wereldwijde fauna en menselijke populaties
Waarom voedingskeuzes een impact hebben op de wereldwijde fauna en menselijke populaties John Tyndall:de vergeten mede-ontdekker van klimaatwetenschap
John Tyndall:de vergeten mede-ontdekker van klimaatwetenschap Groen nationalisme? Hoe extreemrechts kan leren van het milieu te houden
Groen nationalisme? Hoe extreemrechts kan leren van het milieu te houden
Hoofdlijnen
- Hoe dieren genen hergebruiken om beide ledematen en ogen te ontwikkelen
- Routes uit isolatie voor Yellowstone grizzlyberen
- Wat zit er in je tarwe? Wetenschappers voegen het genoom van de meest voorkomende broodtarwe samen
- Hoe een utility-functie af te leiden
- De illegale schildpaddenhandel - waarom wetenschappers geheimen bewaren
- Kan e-learning de dreiging van invasieve uitheemse soorten zoals de Japanse duizendknoop helpen tegengaan?
- Studie geeft inzicht in hoe algen kooldioxide uit de lucht zuigen
- Hoe de pest werkt
- Wat gebeurt er als mitose fout gaat en in welke fase gaat het fout?
De meeste cellen groeien en delen voortdurend. Een proces dat de celcyclus wordt genoemd, laat een cel groeien, zijn DNA dupliceren en delen. Celdeling gebeurt via een ander proc
- In enkele seconden vlees- en visfraude aan het licht brengen met een draagbare MasSpec-pen

- Extreme UV-laser toont de vorming van luchtverontreinigende stoffen

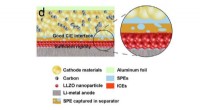
- Onderzoekers ontwerpen dendrietvrije lithiumbatterij
- Wat is het chemische middel dat naar verluidt werd gebruikt om de Russische politicus Alexei Navalny te vergiftigen?

- Ontdekking van hoe mensen de geur van de dood ervaren, kan levens redden

 Dammen staan onder water, het dodental in Zuid-Brazilië blijft stijgen
Dammen staan onder water, het dodental in Zuid-Brazilië blijft stijgen  El Niño hielp dit orkaanseizoen de stormen uit de VS weg te houden. Hoe zit het met volgend jaar?
El Niño hielp dit orkaanseizoen de stormen uit de VS weg te houden. Hoe zit het met volgend jaar?  Wat zijn de voor- en nadelen van doelgerichte steekproeven?
Wat zijn de voor- en nadelen van doelgerichte steekproeven?  Machine learning framework ID's doelen voor het verbeteren van katalysatoren
Machine learning framework ID's doelen voor het verbeteren van katalysatoren Stabiliserende monolaagnitrides met silicium
Stabiliserende monolaagnitrides met silicium Hoe middenmanagers kunnen bijdragen aan een meer rechtvaardige werkplek
Hoe middenmanagers kunnen bijdragen aan een meer rechtvaardige werkplek Onderzoek naar afval op zee telt afval van Texas tot Florida
Onderzoek naar afval op zee telt afval van Texas tot Florida Komt de energie uit verdamping van de zon?
Komt de energie uit verdamping van de zon?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

