
Wetenschap
Hoeveel chemische bindingen kan een enkel atoom van deze elementen waterstof-koolstof-stikstof vormen?
Waterstofatoom heeft één elektron in de buitenste schil, dat een covalente binding kan vormen met een ander atoom om stabiliteit te bereiken. In het geval van water (H2O) vormt elk waterstofatoom bijvoorbeeld één binding met zuurstof.
Koolstof
Eén enkel koolstofatoom kan maximaal vier covalente bindingen vormen. Deze veelzijdigheid is te danken aan de vier valentie-elektronen van koolstof, waardoor het elektronenparen kan delen met maximaal vier andere atomen. In methaan (CH4) deelt koolstof bijvoorbeeld zijn vier valentie-elektronen met vier waterstofatomen, waardoor vier covalente C-H-bindingen worden gevormd.
Stikstof
Stikstof heeft vijf valentie-elektronen en kan doorgaans drie covalente bindingen vormen. Door drie elektronenparen te delen met andere atomen bereikt stikstof een stabiele configuratie. In ammoniak (NH3) vormt elke stikstof bijvoorbeeld drie bindingen met drie waterstofatomen. Stikstof kan echter onder specifieke omstandigheden af en toe vier of zelfs vijf covalente bindingen vormen.
 Overeenkomsten en verschillen tussen kikkers en padden
Overeenkomsten en verschillen tussen kikkers en padden  Team ontdekt een belangrijke rol voor nitraat in het Arctische landschap
Team ontdekt een belangrijke rol voor nitraat in het Arctische landschap Opdoemende klimaateffecten:10 afhaalrestaurants uit het ontwerp-VN-rapport
Opdoemende klimaateffecten:10 afhaalrestaurants uit het ontwerp-VN-rapport Wetenschappers bestuderen hoe grootschalige verstoringen van het milieu oude samenlevingen beïnvloedden
Wetenschappers bestuderen hoe grootschalige verstoringen van het milieu oude samenlevingen beïnvloedden  Antarctische Circumpolaire Stroom stroomt sneller in warme fasen
Antarctische Circumpolaire Stroom stroomt sneller in warme fasen
Hoofdlijnen
- Vreemde ondernemingen:mierenkoninginnen begraven doden om ziekte te voorkomen
- Waren onze tetrapod-voorouders doof?
- Zijn glucose en fructose beide monosachariden?
- Het verschil tussen rode en witte bloedcellen
- Hoe het bewustzijn bij dieren onderzocht zou kunnen worden
- Onderzoekers ontdekken dat twee verschillende ecologische mechanismen veerkracht kunnen bieden tegen invasieve soorten
- Wat hondeneigenaren moeten weten over leptospirose
- Laat DNA de cellen weten wat eiwitten moeten maken?
- Wie controleert wie:Algen of zeeanemoon?
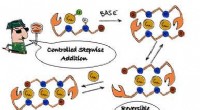
- Moleculaire draden bouwen, één atoom tegelijk
- Enzymen ontwikkelen om het plasticprobleem van de planeet op te lossen

- Wetenschappers ontdekken een verborgen calcium-cholesterolverbinding

- Onderzoekers ontwikkelen een koolstofveer met hoge samendrukbaarheid en rekbaarheid

- Complex levend weefsel bioprinten in slechts enkele seconden

 Een netwerk met twee aanzichten om diepte en egobeweging te voorspellen uit monoculaire sequenties
Een netwerk met twee aanzichten om diepte en egobeweging te voorspellen uit monoculaire sequenties Een microscoop uitfaseren trucs
Een microscoop uitfaseren trucs Aboriginal tradities beschrijven de complexe bewegingen van planeten, de dwalende sterren van de hemel
Aboriginal tradities beschrijven de complexe bewegingen van planeten, de dwalende sterren van de hemel Waarom biodiversiteit belangrijk is en wat de wereld eraan doet
Waarom biodiversiteit belangrijk is en wat de wereld eraan doet  loodgieter, grafenes laatste neef, gerealiseerd op de nano-waterkubus
loodgieter, grafenes laatste neef, gerealiseerd op de nano-waterkubus Ontsnappen aan kinetische vallen:hoe moleculaire interacties het mogelijk maken om de energiebarrière te overwinnen
Ontsnappen aan kinetische vallen:hoe moleculaire interacties het mogelijk maken om de energiebarrière te overwinnen  Wat is verbinding CaCo3?
Wat is verbinding CaCo3?  Is elke verbinding die waterstof bevat een zuur?
Is elke verbinding die waterstof bevat een zuur?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

