
Wetenschap
Wat gebeurt er als een vloeistof het kookpunt bereikt?
Dit gebeurt er als een vloeistof het kookpunt bereikt:
- Bij de gegeven temperatuur en druk zijn de vloeistof en de damp in evenwicht, wat betekent dat ze allebei naast elkaar kunnen bestaan.
- Door de snelle verdamping vormen zich dampbellen in de vloeistof. Deze bellen, samengesteld uit de damptoestand van de vloeistof, worden groter en stijgen naar de oppervlakte.
- Op het oppervlak van de vloeistof barsten de uitzettende dampbellen, waardoor damp in de atmosfeer vrijkomt. Door het vrijkomen van damp ontstaat de schijn van koken en borrelen.
- Naarmate er meer damp vrijkomt, vormen en stijgen er meer bellen, waardoor er voortdurend stoom of damp ontstaat.
Het is belangrijk op te merken dat het kookpunt van een vloeistof afhankelijk is van verschillende factoren, waaronder atmosferische druk, hoogte en onzuiverheden in de vloeistof. Over het algemeen kookt een vloeistof bij een hogere temperatuur naarmate de omgevingsdruk toeneemt en een lagere druk tot lagere kookpunten leidt.
Hoofdlijnen
- Welke term verwijst naar organismen die worden gebruikt om de gezondheid van het milieu te bewaken?
- Uit de kleine teelballen van vliegen ontstaat nieuw inzicht in hoe genen ontstaan
- Waar in uw lichaam komt mitose het vaakst voor?
- Onderzoekers ontleden het DNA van 's werelds grootste zoogdieren om te ontdekken hoe walvissen de kans op kanker trotseren
- Studie ontdekt dat cellulaire activiteit die erop wijst dat recycling in ons DNA zit
- Hoest uw paard? Misschien heeft het astma
- Hoe het influenzavirus efficiënte virale RNA-replicatie bereikt
- Centromeeronderzoek levert nieuwe inzichten op in de mechanismen van chromosoomsegregatiefouten
- Welke functie heeft emb-agar?
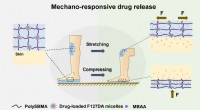
- Mechano-responsieve hydrogel ontwikkeld voor wondgenezing
- Een slimme chemo-enzymatische methode detecteert en verwijdert gevaarlijke fenolen

- Heteractis magnifica zeeanemonen kunnen helpen bij het bestrijden van de ziekte van Alzheimer

- Nieuwe strategie verbetert de stabiliteit van metaalkatalysatoren uit de platinagroep

- Nieuw retroreflecterend materiaal kan worden gebruikt in nachtelijke, van kleur veranderende verkeersborden

 Afbeelding:Hubble bekijkt een sterrenstelsel met vage draden
Afbeelding:Hubble bekijkt een sterrenstelsel met vage draden West-Groenlandse ijskap smelt het snelst in eeuwen
West-Groenlandse ijskap smelt het snelst in eeuwen www@20:Hoe de techneuten de cyberdierentuin temden
www@20:Hoe de techneuten de cyberdierentuin temden  Wat is de toekomst voor Facebook, na een jaar vol schandalen?
Wat is de toekomst voor Facebook, na een jaar vol schandalen?  Tips voor het vermenigvuldigen van radicalen
Tips voor het vermenigvuldigen van radicalen Afbeelding:technici zorgen ervoor dat de zonnekap van James Webb Space Telescopes de stress overleeft die tijdens de lancering wordt ervaren
Afbeelding:technici zorgen ervoor dat de zonnekap van James Webb Space Telescopes de stress overleeft die tijdens de lancering wordt ervaren Onderzoekers bedenken 3D-printer die energetische materialen veiliger kan maken milieuvriendelijker
Onderzoekers bedenken 3D-printer die energetische materialen veiliger kan maken milieuvriendelijker Microben meten het succes van ecologisch herstel
Microben meten het succes van ecologisch herstel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


