
Wetenschap
Is natriumhypochloriet vrij chloor?
Vrij chloor verwijst naar de concentratie van chlooratomen die niet chemisch gebonden zijn aan andere elementen of verbindingen in het water. Wanneer natriumhypochloriet aan water wordt toegevoegd, dissocieert het en vormt hypochloorzuur (HOCl), het belangrijkste desinfecterende type dat verantwoordelijk is voor de zuiverende werking van chloor. HOCl kan verder dissociëren in waterstofionen (H+) en hypochlorietionen (OCl-), waarbij de relatieve verhoudingen van elke soort afhankelijk zijn van de pH van het water.
In de context van waterdesinfectie verwijst vrij chloor specifiek naar de concentratie HOCl en OCl-ionen die in het water aanwezig zijn. De aanwezigheid van vrij chloor garandeert de desinfectie-effectiviteit en resterende bescherming tegen microbiële besmetting. Daarom kan natriumhypochloriet worden beschouwd als een bron van vrij chloor wanneer het aan water wordt toegevoegd en dissocieert om HOCl te vormen.
Het is echter belangrijk op te merken dat de term 'vrij chloor' ook andere chloorverbindingen kan omvatten, zoals chloorgas (Cl2) en chlooramines, die worden gevormd wanneer chloor reageert met stikstofverbindingen in water. Daarom kan de specifieke definitie en samenstelling van vrij chloor variëren afhankelijk van de context en toepassing.
 Analyse van isotopen op nitraat in sake ter bestrijding van drankfraude in Japan
Analyse van isotopen op nitraat in sake ter bestrijding van drankfraude in Japan  Wat is de winningsmethode van chroom?
Wat is de winningsmethode van chroom?  Snelheidsvoorspelling voor homogene nucleatie van methaanhydraat
Snelheidsvoorspelling voor homogene nucleatie van methaanhydraat Hoe kan het Tyndall-effect worden gebruikt om onderscheid te maken tussen een colloïde en een oplossing?
Hoe kan het Tyndall-effect worden gebruikt om onderscheid te maken tussen een colloïde en een oplossing?  Team laat zien hoe uraniumditelluride zelfs bij hoge magnetische velden supergeleidend blijft
Team laat zien hoe uraniumditelluride zelfs bij hoge magnetische velden supergeleidend blijft
 Bossen in Europa en Azië lopen een groter risico op schadelijke koudegolf
Bossen in Europa en Azië lopen een groter risico op schadelijke koudegolf Stedelijke gebieden hebben meer kans op door neerslag veroorzaakte aardverschuivingen, groeiende populaties bloot te stellen aan glijgevaren
Stedelijke gebieden hebben meer kans op door neerslag veroorzaakte aardverschuivingen, groeiende populaties bloot te stellen aan glijgevaren Wetenschapper toont effect van opwarming van de aarde op de uitstoot van broeikasgassen in rijstgronden
Wetenschapper toont effect van opwarming van de aarde op de uitstoot van broeikasgassen in rijstgronden Poll:Amerikanen wijten wild weer aan opwarming van de aarde
Poll:Amerikanen wijten wild weer aan opwarming van de aarde Muziekstreaming heeft een veel grotere ecologische voetafdruk dan de hoogtijdagen van platen en cd's - nieuwe bevindingen
Muziekstreaming heeft een veel grotere ecologische voetafdruk dan de hoogtijdagen van platen en cd's - nieuwe bevindingen
Hoofdlijnen
- Onderzoekers tonen aan dat generalistische soorten ‘manusje-van-alles zijn en alles beheersen’
- Hoe helpen bacteriën in de thee-industrie?
- Waar vindt cellulaire ademhaling plaats?
- Landschaps- en klimaatfactoren kunnen de prevalentie van de ziekte van Lyme voorspellen
- Camera's onthullen dat wombatholen een veilige haven kunnen zijn na brand en waterpoelen na regen
- Een afweermechanisme om darmwormen te doden
- Wetenschappers leggen uit hoe chromosomen zich reorganiseren na celdeling
- Japan Fisheries Agency stelt voor de commerciële vangst van gewone vinvissen toe te staan
- Waarom leven mannen niet zo lang als vrouwen?
- Bestel op! AI vindt het juiste materiaal

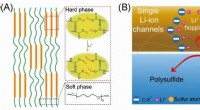
- Stabiliserende zwavelkathode door enkelvoudig Li-ionkanaalpolymeerbindmiddel
- Word wakker en ruik de koffie:onderzoek toont aan dat bevriezing van bonen het aroma kan behouden

- Foto-geïnduceerde ionenverplaatsing in perovskieten met gemengde halogenides voor een batterij die direct door licht kan worden opgeladen

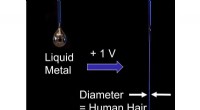
- Beheersing van stromen vloeibaar metaal bij kamertemperatuur
 Hoe biologen veldwerk veiliger en rechtvaardiger maken
Hoe biologen veldwerk veiliger en rechtvaardiger maken Gespiegelde chip kan handheld donkerveldmicroscopen mogelijk maken
Gespiegelde chip kan handheld donkerveldmicroscopen mogelijk maken Ozonherstel kan worden vertraagd door niet-gereguleerde chemicaliën
Ozonherstel kan worden vertraagd door niet-gereguleerde chemicaliën Siliciumqubits plus licht zorgen voor nieuwe kwantumcomputercapaciteit
Siliciumqubits plus licht zorgen voor nieuwe kwantumcomputercapaciteit Waarom moet een buret en pipet worden afgespoeld met de juiste oplossing vóór een titratie?
Waarom moet een buret en pipet worden afgespoeld met de juiste oplossing vóór een titratie?  Wat is elektrolytisch koper?
Wat is elektrolytisch koper?  Leven op de bodem van de Noordelijke IJszee, met strengheid en in detail
Leven op de bodem van de Noordelijke IJszee, met strengheid en in detail NASA vindt zware regen ten zuidwesten van tropische cycloon Uesis center
NASA vindt zware regen ten zuidwesten van tropische cycloon Uesis center
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

