
Wetenschap
Hoe onderscheidt de waterstofkarakteristiek zich van andere elementen uit groep 1?
1. Elektronische configuratie :Waterstof heeft slechts één elektron in de buitenste schil, terwijl andere elementen uit Groep 1 één valentie-elektron hebben. Dit verschil in elektronische configuratie resulteert in significante verschillen in hun chemische eigenschappen. Waterstof kan covalente bindingen vormen door zijn enkele elektron te delen, terwijl andere elementen uit Groep 1 de neiging hebben hun enkele elektron te verliezen om ionische bindingen te vormen.
2. Ionisatie-energie :Waterstof heeft de hoogste ionisatie-energie van de elementen uit Groep 1. Dit betekent dat er meer energie nodig is om een elektron uit waterstof te verwijderen vergeleken met andere Groep 1-elementen. Dit komt doordat de kleine atomaire omvang en de hoge nucleaire lading van waterstof een sterke elektrostatische aantrekkingskracht creëren tussen de kern en het elektron.
3. Elektronegativiteit :Waterstof heeft een hogere elektronegativiteit dan de andere elementen uit Groep 1. Elektronegativiteit meet het vermogen van een atoom om elektronen aan te trekken in een chemische binding. De hogere elektronegativiteit van waterstof betekent dat het een grotere neiging heeft om elektronen naar zichzelf toe te trekken, wat resulteert in meer polaire covalente bindingen.
4. Chemische reactiviteit :Waterstof is zeer reactief, terwijl andere elementen uit Groep 1 minder reactief zijn. De hoge reactiviteit van waterstof is te danken aan de lage ionisatie-energie en de hoge elektronegativiteit. Het reageert gemakkelijk met veel elementen en verbindingen om verschillende soorten verbindingen te vormen, waaronder hydriden, zuren en organische verbindingen.
5. Fysieke eigenschappen :Waterstof heeft unieke fysische eigenschappen vergeleken met andere elementen uit Groep 1. Het is het lichtste en meest voorkomende element in het universum. Onder standaardomstandigheden bestaat waterstof als een diatomisch gas (H2). Het heeft het laagste kookpunt en smeltpunt van de elementen uit groep 1.
Vanwege deze verschillende kenmerken wordt waterstof vaak beschouwd als een aparte categorie binnen het periodiek systeem, in plaats van uitsluitend te worden gegroepeerd met de alkalimetalen (elementen van groep 1).
 Is een chemische verandering van pizzapapier en een ijzeren spijker of een fysieke verandering?
Is een chemische verandering van pizzapapier en een ijzeren spijker of een fysieke verandering?  Nieuwe reactie maakt indoline-steigers beschikbaar voor farmaceutische ontwikkeling
Nieuwe reactie maakt indoline-steigers beschikbaar voor farmaceutische ontwikkeling Is feSO4 een ionische of covalente verbinding?
Is feSO4 een ionische of covalente verbinding?  Wat is de algemene naam voor NH2 · 2CO?
Wat is de algemene naam voor NH2 · 2CO?  Welke symbolen zie je in een laboratorium?
Welke symbolen zie je in een laboratorium?
 Hoogte is belangrijk als het gaat om klimaatverandering, ontbossing en overleving van soorten
Hoogte is belangrijk als het gaat om klimaatverandering, ontbossing en overleving van soorten Bergen zwaaien naar het seismische lied van de aarde
Bergen zwaaien naar het seismische lied van de aarde  Vijvers kunnen meer koolstof opnemen dan bossen. Zo bestrijden ze de klimaatverandering in uw tuin
Vijvers kunnen meer koolstof opnemen dan bossen. Zo bestrijden ze de klimaatverandering in uw tuin  Waarom moerassen de sleutel kunnen zijn tot het bestrijden van klimaatverandering
Waarom moerassen de sleutel kunnen zijn tot het bestrijden van klimaatverandering Wat is de gemiddelde regenval voor een toendra-klimaat?
Wat is de gemiddelde regenval voor een toendra-klimaat?
Hoofdlijnen
- Onderzoek ondersteunt de theorie dat mensen het vermogen hebben ontwikkeld om lange afstanden af te leggen om prooien te vangen
- Hoe veranderde de functie van de voorpoten toen gewervelde dieren ledematen kregen en naar het land trokken?
- Kan een viraal genoom worden gemaakt van zowel DNA als RNA?
- Gemanipuleerde bacteriën zijn veelbelovend voor een duurzame biobrandstofindustrie, zeggen onderzoekers
- Percepties over wat er nodig is om te slagen in STEM-gebieden kunnen vrouwen buitensluiten
- Wat is de elektrische impuls die een Axon naar beneden beweegt?
- Cytoskeleton: definitie, structuur en functie (met diagram)
- Onderzoekers ontsluiten mogelijk pad om vleesetende bacteriën te behandelen
- Kijk hoe bacteriën muteren tot medicijnresistente superbacteriën
- Code voor fijnafstemming van elastomeren om biologische materialen na te bootsen
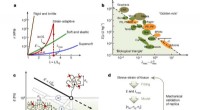
- Een manier om kunstmatige intelligentie te gebruiken om chemische reacties te voorspellen
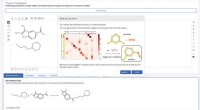
- Atomaire resolutie-eiwitmodellen onthullen nieuwe details over eiwitbinding
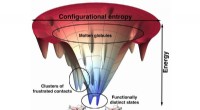
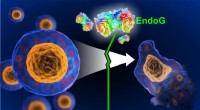
- Biochemici ontdekken een enzym om celdood te stoppen
- Nieuw ontwikkelde ijswerende coating is 100 keer sterker dan andere

 7 geheime grotten die we graag binnen zien
7 geheime grotten die we graag binnen zien  Nieuwe endoscoop gebruikt buigbare GRIN-lens voor 3D-microscopie
Nieuwe endoscoop gebruikt buigbare GRIN-lens voor 3D-microscopie Tientallen gevreesde doden in hittegolf Karachi:liefdadigheid
Tientallen gevreesde doden in hittegolf Karachi:liefdadigheid Krachtige tyfoonbeslagen Okinawa, karnen naar het vasteland van Japan
Krachtige tyfoonbeslagen Okinawa, karnen naar het vasteland van Japan Microgestructureerde optische vezels vinden hun 3D-geprinte groef
Microgestructureerde optische vezels vinden hun 3D-geprinte groef Initiatieven om de digitale kloof te dichten moeten ook na de COVID-19-pandemie werken
Initiatieven om de digitale kloof te dichten moeten ook na de COVID-19-pandemie werken Branden die Brits-Columbia overweldigen; rook verstikt de lucht
Branden die Brits-Columbia overweldigen; rook verstikt de lucht VS gebruiken nep-sociale media om mensen te controleren die land binnenkomen
VS gebruiken nep-sociale media om mensen te controleren die land binnenkomen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

