
Wetenschap
Welke binding ontstaat als een chlooratoom in contact komt met een ander atoom?
Wanneer een chlooratoom in contact komt met een ander atoom, vormen ze een covalente binding. Dit type binding treedt op wanneer twee of meer atomen hun buitenste elektronen delen, waardoor een sterke binding tussen de betrokken atomen ontstaat. In het geval van chloor heeft het zeven elektronen in zijn buitenste schil, en heeft het nog één elektron nodig om zijn octet te voltooien. Wanneer chloor in contact komt met een ander atoom dat een extra elektron heeft, zal het chlooratoom het extra elektron opnemen en er een covalente binding mee vormen. Deze binding wordt gevormd door het covalent delen van elektronen tussen de twee atomen, waardoor een stabiel molecuul of verbinding ontstaat.
 Studie analyseert de ecologische duurzaamheid van diëten bij kinderen en adolescenten
Studie analyseert de ecologische duurzaamheid van diëten bij kinderen en adolescenten  Effecten van koolwaterstoffen op het milieu
Effecten van koolwaterstoffen op het milieu Covid en vervuiling:nauw met elkaar verbonden, samengestelde bedreiging
Covid en vervuiling:nauw met elkaar verbonden, samengestelde bedreiging Opwarmende Groenlandse ijskap passeert point of no return
Opwarmende Groenlandse ijskap passeert point of no return Bodembiologisch onderzoek kan bijdragen aan een duurzamere toekomst
Bodembiologisch onderzoek kan bijdragen aan een duurzamere toekomst
Hoofdlijnen
- Wat is de functie van een rattenmilt?
- Wetenschappers bieden nieuw inzicht in de manier waarop genexpressie wordt gecontroleerd
- Hoe planten defensieve gifstoffen produceren zonder zichzelf schade toe te brengen
- Een knipperende vis onthult aanwijzingen over hoe onze voorouders uit waterland zijn geëvolueerd
- Goed excuus,
- Hoe krijgen mensen stikstof in hun lichaam?
- Hoe evolueert het vermijden van inteelt bij planten?
- De droge gebieden van Californië zijn hotspots van plantendiversiteit
- Wetenschappers ontdekken hoe je gist kunt beschermen tegen schade bij de productie van biobrandstoffen
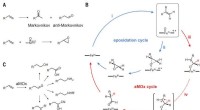
- Gemodificeerd enzym dat wordt gebruikt voor een betere anti-Markovnikov-selectiviteit bij alkeenoxidaties
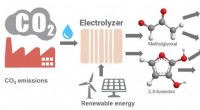
- Hoe klimaatveranderende koolstofdioxide om te zetten in plastic en andere producten?
- Normaal een isolator, diamant wordt een metalen geleider wanneer het wordt blootgesteld aan grote spanning in een nieuw theoretisch model

- Nieuwe moleculaire val reinigt meer radioactief afval van splijtstofstaven

- Wetenschappers verhelderen de kristalstructuur van natriumboride

 Nieuwe theorie over vloeibare kristallen met hoge symmetrie
Nieuwe theorie over vloeibare kristallen met hoge symmetrie Sahara-stofwolk doemt op boven Cuba, Caraïben en Florida
Sahara-stofwolk doemt op boven Cuba, Caraïben en Florida Het 'Puss in Boots'-effect:hoe de ooggrootte van een hond de stemhoogte van een vrouw verandert
Het 'Puss in Boots'-effect:hoe de ooggrootte van een hond de stemhoogte van een vrouw verandert  Wetenschappers ontwikkelen een op deep learning gebaseerd biosensorplatform om virale deeltjes beter te tellen
Wetenschappers ontwikkelen een op deep learning gebaseerd biosensorplatform om virale deeltjes beter te tellen  Soorten slangen in Delaware
Soorten slangen in Delaware  Industrieklaar proces maakt kunststoffen chemisch uit plantensuikers
Industrieklaar proces maakt kunststoffen chemisch uit plantensuikers De Rolling Fourier-ringcorrelatiemethode brengt de lokale kwaliteit in kaart op superresolutieschaal
De Rolling Fourier-ringcorrelatiemethode brengt de lokale kwaliteit in kaart op superresolutieschaal  Afbeelding:Bepi voor de spatie
Afbeelding:Bepi voor de spatie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

