
Wetenschap
Wat gebeurt er als het oxideatoom een zuurstofatoom wordt?
Het verlies van een elektron door een oxide-atoom kan verschillende gevolgen hebben, afhankelijk van het specifieke oxide-atoom en de omgeving waarin het wordt aangetroffen. In sommige gevallen kan het verlies van een elektron ervoor zorgen dat het oxide-atoom reactiever en onstabieler wordt, terwijl het in andere gevallen het oxide-atoom stabieler en inert kan maken.
Als een ijzeroxide-atoom bijvoorbeeld een elektron verliest, kan het reactiever worden en vatbaarder voor corrosie. Dit is de reden waarom ijzeren voorwerpen die worden blootgesteld aan zuurstof en vocht vaak roesten. Aan de andere kant, als een siliciumoxide-atoom een elektron verliest, kan het stabieler worden en beter bestand tegen corrosie. Daarom wordt siliciumdioxide (SiO2) gebruikt als beschermende coating voor veel materialen.
De oxidatie van oxideatomen kan ook een aanzienlijke impact hebben op de eigenschappen van materialen. De oxidatie van titaniumoxide (TiO2) kan er bijvoorbeeld voor zorgen dat het een halfgeleider wordt, wat het bruikbaar maakt in een verscheidenheid aan elektronische apparaten. Op dezelfde manier kan de oxidatie van zinkoxide (ZnO) ervoor zorgen dat het een piëzo-elektrisch materiaal wordt, wat betekent dat het een elektrische lading genereert wanneer het wordt blootgesteld aan mechanische spanning.
Samenvattend kan de oxidatie van oxide-atomen verschillende gevolgen hebben, afhankelijk van het specifieke oxide-atoom en de omgeving waarin het wordt aangetroffen. Enkele van deze gevolgen zijn onder meer verhoogde reactiviteit, verhoogde stabiliteit en veranderingen in de eigenschappen van materialen.
Hoofdlijnen
- Westerse steden proberen te voorkomen dat hongerige beren ravage aanrichten
- Wetenschappers ontdekken fossielen van gigantische zeehagedis die 66 miljoen jaar geleden over de oceanen heerste
- Welke hormonen produceert de hypofyse?
- Welke groepen mensen hebben de neiging hun IQ te overschatten?
- UITLEGGER:Wat is een derecho?
- Hoe de genoomdiversiteit van belangrijke gewassen hun evolutie vertelt
- Vijf redenen om de insecten in je tuin niet te besproeien
- Je bent wat je eet:Biologen brengen genetische routes van op voeding gebaseerde soorteigenschappen in kaart
- Hoe insecten verschillende suikers uit elkaar houden
- Zelfherstellende katalysatoren maken het gemakkelijker om zonne-energie op te slaan met water
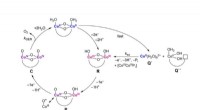
- Nieuwe techniek zet ammoniak naadloos om in groene waterstof
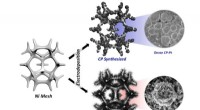
- Hoe verleng je de levensduur van smeermiddelen?

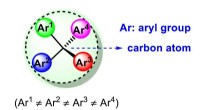
- Wetenschappers hebben nieuwe manier gevonden om chirale tetraarylmethaan te synthetiseren
- Onderzoekers ontwikkelen een eenvoudigere en snellere manier om te kwantificeren, verken therapeutische eiwitten

 De mysteries van DNA-origami ontrafelen
De mysteries van DNA-origami ontrafelen Nieuwe doorbraak laat zien hoe korte lichtpulsen deeltjes vernietigen
Nieuwe doorbraak laat zien hoe korte lichtpulsen deeltjes vernietigen  Ounces converteren naar Mililiters
Ounces converteren naar Mililiters WhatsApp verdedigt encryptie aangezien het meer dan 2 miljard gebruikers heeft
WhatsApp verdedigt encryptie aangezien het meer dan 2 miljard gebruikers heeft Komeetaanval zou PETM kunnen verklaren,
Komeetaanval zou PETM kunnen verklaren,  Staat een goede opkomst gelijk aan goede cijfers?
Staat een goede opkomst gelijk aan goede cijfers? Hoe maak je klimaatactie populair
Hoe maak je klimaatactie populair Jet in de atmosfeer van Jupiter blijkt in perioden van ongeveer vier jaar te fluctueren
Jet in de atmosfeer van Jupiter blijkt in perioden van ongeveer vier jaar te fluctueren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


