
Wetenschap
Waarom is C2H4-ethyleen niet-polair?
C2H4 is ethyleen, ook wel etheen genoemd, is niet apolair. Het is een niet-polair molecuul maar heeft polaire bindingen. Dit komt omdat de elektronegativiteitswaarden van koolstof en waterstof vrijwel gelijk zijn. Daarom worden de elektronen in de C-H-binding vrijwel gelijk verdeeld tussen de twee atomen, en is er geen significante gedeeltelijke lading op beide atoom. Dit resulteert in een niet-polair molecuul. Het molecuul als geheel is echter polair vanwege de aanwezigheid van de dubbele binding tussen de twee koolstofatomen. De dubbele binding creëert een gebied met een hoge elektronendichtheid tussen de twee koolstofatomen, waardoor het molecuul een netto negatieve lading krijgt. Deze negatieve lading wordt gecompenseerd door de twee positieve ladingen op de waterstofatomen, wat resulteert in een polair molecuul.
 Wat maakt een kiemwortel anders dan een molecuul?
Wat maakt een kiemwortel anders dan een molecuul?  Uit onderzoek blijkt precies hoe goedkope brandstofcelkatalysatoren werken
Uit onderzoek blijkt precies hoe goedkope brandstofcelkatalysatoren werken  Wetenschappers ontwikkelen oplossing voor het voorbereiden van macroscopische 2-D MXenes
Wetenschappers ontwikkelen oplossing voor het voorbereiden van macroscopische 2-D MXenes In een auto-accu wordt een zure oplossing genoemd?
In een auto-accu wordt een zure oplossing genoemd?  Onderzoekers identificeren onverwachte wendingen bij het ontwikkelen van nieuwe op polymeren gebaseerde halfgeleiders
Onderzoekers identificeren onverwachte wendingen bij het ontwikkelen van nieuwe op polymeren gebaseerde halfgeleiders
 Kusterosie is niet te stoppen. Dus hoe leven we ermee?
Kusterosie is niet te stoppen. Dus hoe leven we ermee? Onderzoek wijst uit dat arseen tientallen jaren na het einde van de blootstelling kanker kan veroorzaken
Onderzoek wijst uit dat arseen tientallen jaren na het einde van de blootstelling kanker kan veroorzaken Studie laat zien hoe een klein zeedier zichzelf en de oceaan voedt
Studie laat zien hoe een klein zeedier zichzelf en de oceaan voedt Parijs om vervuilingsvrij transport te bestuderen
Parijs om vervuilingsvrij transport te bestuderen India's hoogste rechtbank beveelt stoppelverbranding te stoppen terwijl Delhi zich verslikt
India's hoogste rechtbank beveelt stoppelverbranding te stoppen terwijl Delhi zich verslikt
Hoofdlijnen
- Abelisauroid, een dinosaurus met zeer kleine armen, geïdentificeerd in Argentinië
- Wat is de rol van biogeochemie?
- Je bent wat je eet is net zo belangrijk voor vissen als voor mensen
- Een membraan dat sommige stoffen doorlaat en andere uitsluit, zou een?
- Hoe brengt het gezin cultuur over?
- Wat zijn organellen in een prokaryotische cel?
- IJsberen die rendieren eten:normaal gedrag of gevolg van klimaatverandering?
- Fossiele kikkers delen hun huidverzorgingsgeheimen:analyse van 45 miljoen jaar oude zachte weefsels
- Welk voedsel is geen functie-eiwit?
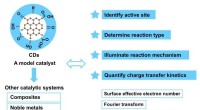
- Geavanceerde multifunctionele koolstofpunten in op foto-elektrochemie gebaseerde energieconversie
- Extreme verbetering van koolwaterstofvergassing via mechanochemie

- Macromoleculaire kristallografie werpt licht op een nieuwe manier om de malariaparasiet aan te pakken

- Directe synthese van waterstofperoxide met behulp van TS-1-ondersteunde katalysatoren
- Wetenschappers ontwikkelen betere beeldvormingstool om ziekten te bestuderen

 Gouden nanodeeltjes om neuronen te redden van celdood
Gouden nanodeeltjes om neuronen te redden van celdood Met het Mars-methaanmysterie onopgelost, Nieuwsgierigheid dient wetenschappers een nieuwe:zuurstof
Met het Mars-methaanmysterie onopgelost, Nieuwsgierigheid dient wetenschappers een nieuwe:zuurstof Onderzoek onthult dat waargenomen gendervooroordelen tegen vrouwen een dominante factor zijn bij de belangrijkste keuze van de universiteit
Onderzoek onthult dat waargenomen gendervooroordelen tegen vrouwen een dominante factor zijn bij de belangrijkste keuze van de universiteit Zijn dierentuinen onbedoeld medeplichtig aan de handel in wilde dieren? Het geval van een zeldzame Borneo-hagedis
Zijn dierentuinen onbedoeld medeplichtig aan de handel in wilde dieren? Het geval van een zeldzame Borneo-hagedis  Hoe stemvorken werken
Hoe stemvorken werken  Hoe T-scores naar Percentielen worden geconverteerd
Hoe T-scores naar Percentielen worden geconverteerd  Een keramische aerogel gemaakt met nanokristallen en ingebed in een matrix voor gebruik in thermische isolatietoepassingen
Een keramische aerogel gemaakt met nanokristallen en ingebed in een matrix voor gebruik in thermische isolatietoepassingen Recordbrekende terahertz-laserstraal
Recordbrekende terahertz-laserstraal
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

