
Wetenschap
Hoe beïnvloedt de toevoeging van opgeloste stoffen het waterpotentieel?
De omvang van de afname van het waterpotentieel hangt af van de concentratie van de opgeloste stof. Hoe geconcentreerder de oplossing, hoe lager het waterpotentieel. Dit komt omdat er meer opgeloste deeltjes zijn die concurreren met watermoleculen om waterstofbinding, waardoor er minder watermoleculen vrij blijven om te bewegen.
Het effect van opgeloste stoffen op het waterpotentieel is belangrijk in veel biologische processen. De toevoeging van opgeloste stoffen aan de bodem kan er bijvoorbeeld voor zorgen dat planten verwelken omdat het waterpotentieel van de bodem lager wordt dan het waterpotentieel van de plant. Hierdoor kan de plant moeilijk water opnemen.
De toevoeging van opgeloste stoffen kan ook worden gebruikt om voedsel te conserveren. De hoge concentratie opgeloste stoffen in voedingsmiddelen zoals jam en gelei voorkomt de groei van bacteriën en andere micro-organismen, omdat het waterpotentieel van het voedsel te laag is om hun groei te ondersteunen.
Hier is een wiskundige vergelijking die de relatie beschrijft tussen de concentratie opgeloste stoffen en het waterpotentieel:
```
Ψw =Ψw° - CᵢRT
```
Waar:
- Ψw is het waterpotentieel
- Ψw° is het waterpotentieel van zuiver water
- Cᵢ is de concentratie van de opgeloste stof
- R is de ideale gasconstante
- T is de temperatuur in Kelvin
 Kleurmix-verfactiviteiten voor kleuters
Kleurmix-verfactiviteiten voor kleuters Nieuwe microfluïdische chip verhoogt de gevoeligheid van immunoassays met 1000x
Nieuwe microfluïdische chip verhoogt de gevoeligheid van immunoassays met 1000x Celtoxinen nader bekeken:Onderzoekers onderzoeken hoe radionucliden interageren met niercellen
Celtoxinen nader bekeken:Onderzoekers onderzoeken hoe radionucliden interageren met niercellen  Hoe Borax Powder
Hoe Borax Powder Elektrochemie opent nieuwe toegang tot belangrijke klassen van stoffen
Elektrochemie opent nieuwe toegang tot belangrijke klassen van stoffen
 Tropische cycloon Ella verpakt in NASA-beelden
Tropische cycloon Ella verpakt in NASA-beelden Bijproduct van bier vermengd met mest blijkt een uitstekend bestrijdingsmiddel
Bijproduct van bier vermengd met mest blijkt een uitstekend bestrijdingsmiddel Seychellen-chef roept vanuit de diepte voor bescherming van de oceaan
Seychellen-chef roept vanuit de diepte voor bescherming van de oceaan Nieuw rapport over klimaatverandering wordt waarschijnlijk tot de dood genegeerd
Nieuw rapport over klimaatverandering wordt waarschijnlijk tot de dood genegeerd Wetenschappers vinden ijzersneeuw in de kern van de aarde
Wetenschappers vinden ijzersneeuw in de kern van de aarde
Hoofdlijnen
- 4 manieren om te vertellen of gezondheidsrapportage nepnieuws kan zijn
- Beschermende en ondersteunende structuur die het celmembraan omringt in planten en sommige bacteriën?
- Sluwe kraaien weten wat er nodig is om een goed stuk gereedschap te maken
- Heeft kunstmatige intelligentie u krediet ontzegd?
- Wat maakt bruine rijst gezond? Het decoderen van de chemie van zijn voedingsrijkdom
- Kleine bijen spelen een grote rol in het geheime seksleven van bomen
- Studie beslecht 125 jaar durend debat over hoe stikstofbindende bacteriën de celwanden van peulvruchten doorbreken
- Onderzoekers ontdekken de sleutel tot het moleculaire mysterie van hoe planten reageren op veranderende omstandigheden
- Kan ik hier doorheen glippen? Hoe sommige schimmels kleine gaatjes kunnen laten groeien
- Wanneer meer botvormende cellen gelijk zijn aan minder bot

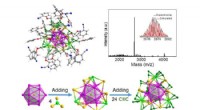
- Wetenschappers bouwen M29-clustermodelkatalysator
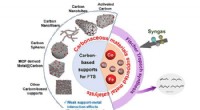
- Op koolstof gebaseerde katalysatoren die worden gebruikt voor Fischer-Tropsch-synthese
- Visualisatie van moleculaire beweging van gesubstitueerd 9-fosfaanthraceen

- Kunstmatige antimicrobiële peptiden kunnen helpen om resistente bacteriën te overwinnen
 Een neutraal atoom heeft atoomnummer 12 en massa 24. Hoeveel elektronen bevat het?
Een neutraal atoom heeft atoomnummer 12 en massa 24. Hoeveel elektronen bevat het?  Op grafeen gebaseerde implanteerbare technologie maakt de weg vrij voor uiterst nauwkeurige therapeutische toepassingen
Op grafeen gebaseerde implanteerbare technologie maakt de weg vrij voor uiterst nauwkeurige therapeutische toepassingen  Onderzoekers verzamelen numeriek bewijs van kwantumchaos in het Sachdev-Ye-Kitaev-model
Onderzoekers verzamelen numeriek bewijs van kwantumchaos in het Sachdev-Ye-Kitaev-model Golfinterferentie: constructief en destructief (met voorbeelden)
Golfinterferentie: constructief en destructief (met voorbeelden)  Zijn chemische raketten of zonnezeilen beter in het terugwinnen van grondstoffen uit asteroïden?
Zijn chemische raketten of zonnezeilen beter in het terugwinnen van grondstoffen uit asteroïden?  Noodzaak is inderdaad de moeder van de uitvinding - ongeacht de middelen, studie toont
Noodzaak is inderdaad de moeder van de uitvinding - ongeacht de middelen, studie toont Is het Amerikaanse olietijdperk al aan het afnemen?
Is het Amerikaanse olietijdperk al aan het afnemen?  Longorganoïden onthullen hoe ziekteverwekkers menselijk longweefsel infecteren
Longorganoïden onthullen hoe ziekteverwekkers menselijk longweefsel infecteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

