
Wetenschap
Wat is een fysieke eigenschap van een gigantische covalente structuur?
1. Sterk en stijf: De sterke covalente bindingen tussen atomen in gigantische covalente structuren resulteren in robuuste en stijve materialen. De dicht opeengepakte rangschikking van atomen, vaak in regelmatige patronen, vergroot hun stijfheid verder. Diamant, samengesteld uit koolstofatomen gerangschikt in een kubusvormig diamantrooster, staat bijvoorbeeld bekend om zijn uitzonderlijke hardheid en krasbestendigheid.
2. Hoge smelt- en kookpunten: Gigantische covalente structuren hebben over het algemeen hoge smelt- en kookpunten vanwege de sterke cohesiekrachten die hun atomen bij elkaar houden. Het overwinnen van deze krachten vereist aanzienlijke energie, wat leidt tot verhoogde smelt- en kookpunten. Grafiet, een andere vorm van koolstof, smelt bijvoorbeeld bij ongeveer 3642°C, en siliciumcarbide (SiC) smelt bij ongeveer 2730°C.
3. Slechte elektrische geleidbaarheid: Over het algemeen zijn gigantische covalente structuren slechte elektriciteitsgeleiders. Omdat de valentie-elektronen in deze structuren stevig gebonden zijn aan hun respectieve atomen, zijn ze niet gemakkelijk te mobiliseren. Ze missen dus de vrije elektronen die nodig zijn voor een efficiënte elektrische geleiding. Diamant is bijvoorbeeld een uitstekende elektrische isolator.
4. Transparantie: Bepaalde gigantische covalente structuren, zoals diamant, zijn transparant voor zichtbaar licht vanwege hun regelmatige en symmetrische rangschikking van atomen. Het ontbreken van gemakkelijk exciteerbare elektronen verhindert dat ze licht in het zichtbare bereik absorberen, waardoor licht door kan gaan zonder noemenswaardige absorptie. Deze eigenschap maakt diamant waardevol voor diverse optische toepassingen, waaronder precisiesnijgereedschappen en laservensters.
5. Broosheid: Ondanks hun sterkte zijn gigantische covalente structuren vaak broos, wat betekent dat ze plotseling breken zonder noemenswaardige plastische vervorming wanneer ze worden blootgesteld aan spanning. De rigide aard van de covalente bindingen beperkt de beweging en herschikking van atomen onder uitgeoefende krachten, waardoor hun vermogen om vervorming te weerstaan wordt beperkt. Broze materialen zoals diamant en siliciumcarbide breken gemakkelijk wanneer ze worden blootgesteld aan overmatige of plaatselijke spanning.
Door deze fysieke eigenschappen te begrijpen, kunnen wetenschappers en ingenieurs gigantische covalente materialen effectief gebruiken op verschillende gebieden, waaronder techniek, constructie, optica, elektronica en materiaalkunde. De unieke combinatie van sterkte, stijfheid, transparantie en andere eigenschappen maakt deze materialen essentieel voor een breed scala aan toepassingen, van hoogwaardige snijgereedschappen tot componenten die bestand zijn tegen hoge temperaturen en elektronische apparaten.
 Zoutvervuiling beheren om drinkwaterbronnen en zoetwaterecosystemen te beschermen
Zoutvervuiling beheren om drinkwaterbronnen en zoetwaterecosystemen te beschermen De machtige kustsequoia's zijn geboren om te veranderen. Maar kunnen ze snel genoeg evolueren om de opwarming van het klimaat te overleven?
De machtige kustsequoia's zijn geboren om te veranderen. Maar kunnen ze snel genoeg evolueren om de opwarming van het klimaat te overleven?  Emissies van cannabisteeltfaciliteiten kunnen de luchtkwaliteit binnenshuis en in de regio beïnvloeden
Emissies van cannabisteeltfaciliteiten kunnen de luchtkwaliteit binnenshuis en in de regio beïnvloeden Video:Permafrost in het noordpoolgebied - wat stijgende temperaturen betekenen voor de planeet
Video:Permafrost in het noordpoolgebied - wat stijgende temperaturen betekenen voor de planeet Wanneer weten we dat we buitenaards leven hebben gevonden?
Wanneer weten we dat we buitenaards leven hebben gevonden?
Hoofdlijnen
- Welke kenmerken hebben alle prokaryoten gemeen?
- Hoe orbitale diagrammen te doen
- Citroenfruit versterken om beter bestand te zijn tegen klimaatverandering
- Elektrische 'Batmobile' laat zien hoe Chinezen de supercarmarkt in hun vizier hebben
- Hoe komen virussen in cellen? Hun infectietactieken bepalen of ze over soorten heen kunnen springen of een pandemie kunnen veroorzaken
- Wat is de functie van substage in de microscoop?
- Waarom zien mitochondriën er zo uit?
- Coeliakie-vriendelijke ontbijtgranen? Onderzoek toont aan dat haver het antwoord kan zijn
- Hoe cellen snel uitsteeksels creëren voor verkenning en beweging
- Anisotropie van oppervlakteoxidevorming beïnvloedt de voorbijgaande activiteit van een oppervlaktereactie
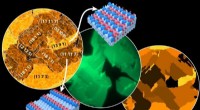
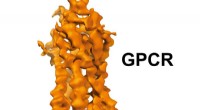
- Cryo-EM onthult interactie tussen belangrijke medicijndoelen
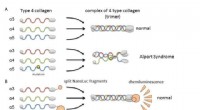
- Nieuwe katalysator zet vervuilende stof om in brandstof

- Een zeer gevoelig en multi-analytisch systeem voor erfelijke nierziekte
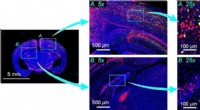
- Optisch beeldvormingssysteem kan een ongekend aantal cellen in een enkele afbeelding vastleggen
 Voorbeelden van natuurrampen en de veranderingen in het milieu Incurred
Voorbeelden van natuurrampen en de veranderingen in het milieu Incurred Dubbel probleem:overstromingen en COVID-19 zijn samengesmolten en vormen een groot gevaar voor Oost-Timor
Dubbel probleem:overstromingen en COVID-19 zijn samengesmolten en vormen een groot gevaar voor Oost-Timor Kunnen oliën uit algen de grootschalige, goedkope productie van biobrandstoffen ondersteunen?
Kunnen oliën uit algen de grootschalige, goedkope productie van biobrandstoffen ondersteunen?  Een iPhone met drie camera's? Het is misschien een van de drie nieuwe modellen voor 2019, rapport zegt
Een iPhone met drie camera's? Het is misschien een van de drie nieuwe modellen voor 2019, rapport zegt Natuurkundigen verhitten vrijstaand grafeen om de kromming van rimpelingen te beheersen
Natuurkundigen verhitten vrijstaand grafeen om de kromming van rimpelingen te beheersen Klaar voor de Galaxy S10? Samsung organiseert 'Unpacked' persevenement op 20 februari
Klaar voor de Galaxy S10? Samsung organiseert 'Unpacked' persevenement op 20 februari  Nieuwe klasse zonnecellen, gebruik van loodvrije perovskietmaterialen
Nieuwe klasse zonnecellen, gebruik van loodvrije perovskietmaterialen Onverwacht gedrag gezien bij efficiënte katalysatoren voor schone energie
Onverwacht gedrag gezien bij efficiënte katalysatoren voor schone energie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

