
Wetenschap
Waarom is koolstofdioxide beter oplosbaar bij hoge druk?
Dit komt omdat wanneer de druk van een gas wordt verhoogd, de moleculen van het gas dichter bij elkaar worden gedwongen, waardoor ze gemakkelijker in de vloeistof kunnen oplossen. De verhoogde druk verhoogt ook het aantal botsingen tussen de gasmoleculen en de vloeibare moleculen, waardoor de kans groter wordt dat de gasmoleculen door de vloeistof worden geabsorbeerd.
In het geval van kooldioxide is het beter oplosbaar bij hoge druk, omdat de kooldioxidemoleculen bij hogere drukken dichter bij elkaar worden gedrukt, waardoor ze gemakkelijker in de vloeistof kunnen oplossen. Bovendien verhoogt de verhoogde druk het aantal botsingen tussen de kooldioxidemoleculen en de watermoleculen, waardoor de kans groter wordt dat de kooldioxidemoleculen door het water worden geabsorbeerd.
 Lichaamsbeweging is goed voor je huid:een eiwit bootst sommige anti-aging effecten bij muizen na
Lichaamsbeweging is goed voor je huid:een eiwit bootst sommige anti-aging effecten bij muizen na Vloeibare schokdempers
Vloeibare schokdempers Lab onthult nieuw werkingsmechanisme tegen SARS-CoV-2 door antiviraal medicijn remdesivir
Lab onthult nieuw werkingsmechanisme tegen SARS-CoV-2 door antiviraal medicijn remdesivir Wat is de reactie tussen natriumhydroxide en calciumbicarbonaat?
Wat is de reactie tussen natriumhydroxide en calciumbicarbonaat?  Effecten van Fenton-achtige reacties van ijzeroxalaat op atmosferische oxidatieprocessen en stralingsforcering
Effecten van Fenton-achtige reacties van ijzeroxalaat op atmosferische oxidatieprocessen en stralingsforcering
 Nieuwe bodemmodellen kunnen atmosferische kooldioxide verminderen, klimaatverandering
Nieuwe bodemmodellen kunnen atmosferische kooldioxide verminderen, klimaatverandering Hoe vertel je een vrouwelijke en mannelijke tijger apart
Hoe vertel je een vrouwelijke en mannelijke tijger apart Oceaantemperaturen beïnvloeden het Midden-Amerikaanse klimaat meer dan ooit gedacht
Oceaantemperaturen beïnvloeden het Midden-Amerikaanse klimaat meer dan ooit gedacht Europese kolonisatie versnelde erosie vertienvoudigd
Europese kolonisatie versnelde erosie vertienvoudigd Rotsachtige ijsbergen en diepe ankers - nieuw onderzoek naar hoe planetaire krachten het aardoppervlak vormen
Rotsachtige ijsbergen en diepe ankers - nieuw onderzoek naar hoe planetaire krachten het aardoppervlak vormen
Hoofdlijnen
- In welk seizoen vindt de kieming van planten plaats?
- Geluidsoverlast schaadt dieren, en we weten niet eens hoeveel
- Team brengt in kaart hoe autofagie functioneert bij zoogdieren; SARS-CoV-2-infectie kan het proces verstoren
- Hoe E. coli veilig door maagzuur gaat
- Een gemakkelijke manier om de schedelzenuwen te leren
- Wat zijn de twee hoofdfasen van de celcyclus?
- Hoe dopamine helpt om sommige voedingsmiddelen verslavend te maken
- Wat zit er in een naam? Een glimp van de evolutie, het benoemen van baby's, het kiezen van een hond, studievondsten
- Van welk systeem is de schedel onderdeel?
- Computationele strategieën overwinnen obstakels bij de ontwikkeling van peptidetherapieën

- Hybride indium-lithiumanoden zorgen voor snel grensvlak-ionentransport
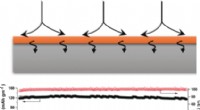
- Onderzoek suggereert dat polymeercomposiet kan dienen als lichter, niet-giftige stralingsafscherming

- Papierspoor leidt tot ontdekkingen van hartkleppen

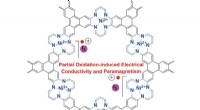
- Nieuw 2D metalen organisch raamwerk met interessante elektrische geleidbaarheid en magnetische eigenschappen
 Onder druk:eiwit-nabootsende moleculen manipuleren met hydrostatische druk
Onder druk:eiwit-nabootsende moleculen manipuleren met hydrostatische druk De draad spoelen voor een zelfgemaakte generator
De draad spoelen voor een zelfgemaakte generator Trillingsenergie het geheim van zelfaangedreven elektronica
Trillingsenergie het geheim van zelfaangedreven elektronica Vraagtekens bij het verband tussen vervuiling door magnetietdeeltjes en de ziekte van Alzheimer
Vraagtekens bij het verband tussen vervuiling door magnetietdeeltjes en de ziekte van Alzheimer Welke informatie krijg je uit chemische vergelijkingen?
Welke informatie krijg je uit chemische vergelijkingen?  Een worstelende recyclingindustrie wordt geconfronteerd met een nieuwe crisis met coronavirus
Een worstelende recyclingindustrie wordt geconfronteerd met een nieuwe crisis met coronavirus Manieren om het ecologische evenwicht te handhaven
Manieren om het ecologische evenwicht te handhaven De milieuvoordelen van een voedseldeeleconomie zijn sterk afhankelijk van de manier waarop het bespaarde geld vervolgens wordt gebruikt
De milieuvoordelen van een voedseldeeleconomie zijn sterk afhankelijk van de manier waarop het bespaarde geld vervolgens wordt gebruikt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

